
| A. | HF MgCl2 NH4Cl | B. | H2S Na2O ? CO2 | ||
| C. | CaCl2 ? NaOH C H4 | D. | NH3 H2O CS2 |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,酸、部分盐、部分碱、非金属氧化物、非金属多原子单质中都含有共价键,部分碱、部分盐和金属氧化物中含有离子键.
解答 解:A.MgCl2中只含离子键、HF中只含共价键,NH4Cl中既有离子键又有共价键,所以化学键类型不同,故A错误;
B.H2S和CO2都只存在共价键,所以化学键类型相同,Na2O是离子键,所以化学键类型不同,故B错误;
C.C H4中只含共价键、CaCl2 中只含离子键,NaOH中既有离子键又有共价键,所以化学键类型不同,故C错误;
D.NH3、H2O和CS2中只含共价键,所以三者化学键类型相同,故D正确;
故选D.
点评 本题考查了离子键和共价键的判断,明确离子键和共价键的区别即可解答,属于基础题,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{2}^{3}$He和${\;}_{2}^{4}$He互为同位素 | |
| B. | ${\;}_{2}^{4}$He原子核内含有4个质子 | |
| C. | ${\;}_{2}^{3}$He原子核内含有3个中子 | |
| D. | ${\;}_{2}^{4}$He的最外层电子数为2,金属性较强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
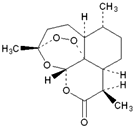 2015年我国女科学家屠呦呦因发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命而荣获诺贝尔奖.青蒿素结构式如图所示,下列关于青蒿素的说法不正确的是( )
2015年我国女科学家屠呦呦因发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命而荣获诺贝尔奖.青蒿素结构式如图所示,下列关于青蒿素的说法不正确的是( )| A. | 难溶于水,易溶于乙醚 | B. | 在热的NaOH溶液中可发生水解反应 | ||
| C. | 一定条件下能与氯气发生取代反应 | D. | 化学式为C15H21O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的压强 | |
| B. | 混合气体的密度 | |
| C. | 当B、C、D三种物质,它们的物质的量nB:nC:nD=2:1:1 | |
| D. | 混合气体的总物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.0l mol•L-1•s-1 | B. | 0.002 mol•L-1•s-1 | ||
| C. | 0.06mol•L-•1s-1 | D. | 0.0025mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ①⑥ | C. | ④⑥ | D. | ⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
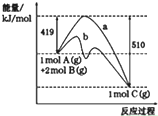
| A. | 曲线b表示使用催化剂后的能量变化 | |
| B. | 正反应活化能大于逆反应活化能 | |
| C. | 由图可知该反应的焓变△H=+91 kJ•mol-1 | |
| D. | 反应中将气体A换为固体反应,其他条件不变,反应放出热量大于91kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CsOH是一种既可与强酸又可与强碱反应的两性氢氧化物 | |
| B. | Cs在空气中燃烧可生成Cs2O和Cs2O2 | |
| C. | Cs与水反应,能发生爆炸,并放出H2 | |
| D. | CsOH很稳定,加热不易分解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com