
【题目】[化学——选修5:有机化学基础]
Prolitane是一种抗抑郁药物,以芳香烃A为原料的合成路线如下:

请回答以下问题:
(1)D的化学名称为___________,D→E的反应类型为___________。
(2)G的官能团名称为___________。
(3)B的结构简式为______________________。
(4)F→G的化学方程式为______________________。
(5)X是D的同系物,ⅹ分子比D分子少一个碳原子,且能发生银镜反应,则满足此条件的X共有___________种(不含立体异构);其屮核磁共振氢谱显示为5组峰,其峰面积比为3︰2︰2︰2︰1,写出符合该要求的Ⅹ的一种同分异构体的结构简式:______________________。
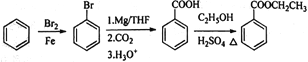
(6)参照 Prolitane的合成路线,设计一条由苯和乙醇为原料制备苯甲酸乙酯的合成路线(其他无机试剂和溶剂任选)。____________________________________________。
【答案】苯乙酸乙酯 取代反应 羰基(或酮基) ![]()
 14
14 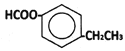 (或
(或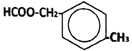 )
) 
【解析】
由合成路线可知,A和氯气光照发生取代反应生成B(C7H7Cl),由C的结构简式可推知B的结构简式为![]() ,结合A的相对分子质量为92,可推知A为甲苯;C和乙醇发生酯化反应生成D,D和CH3CH2COCl发生取代反应生成E,E水解生成F(C11H12O3),F加热脱羧生成G,可推出F的结构简式为
,结合A的相对分子质量为92,可推知A为甲苯;C和乙醇发生酯化反应生成D,D和CH3CH2COCl发生取代反应生成E,E水解生成F(C11H12O3),F加热脱羧生成G,可推出F的结构简式为 ;G和
;G和![]() 发生先加成后消去生成H,H加氢还原得到Prolitane,据此解答。
发生先加成后消去生成H,H加氢还原得到Prolitane,据此解答。
由合成路线可知,A和氯气光照发生取代反应生成B(C7H7Cl),由C的结构简式可推知B的结构简式为![]() ,结合A的相对分子质量为92,可推知A为甲苯;C和乙醇发生酯化反应生成D,D和CH3CH2COCl发生取代反应生成E,E水解生成F(C11H12O3),F加热脱羧生成G,可推出F的结构简式为
,结合A的相对分子质量为92,可推知A为甲苯;C和乙醇发生酯化反应生成D,D和CH3CH2COCl发生取代反应生成E,E水解生成F(C11H12O3),F加热脱羧生成G,可推出F的结构简式为 ;G和
;G和![]() 发生先加成后消去生成H,H加氢还原得到Prolitane,
发生先加成后消去生成H,H加氢还原得到Prolitane,
(1)D的结构简式为 ,化学名称为苯乙酸乙酯;D和CH3CH2COCl发生取代反应生成E,故D→E的反应类型为取代反应,
,化学名称为苯乙酸乙酯;D和CH3CH2COCl发生取代反应生成E,故D→E的反应类型为取代反应,
故答案为:苯乙酸乙酯;取代反应;
(2) G的结构简式为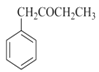 ,含有官能团名称为羰基,
,含有官能团名称为羰基,
故答案为:羰基;
(3) A和氯气光照发生取代反应生成B(C7H7Cl),由C的结构简式可知B的结构简式为![]() 。
。
故答案为:![]() ;
;
(4) F加热脱羧生成G,可推出F的结构简式为 ,所以F→G的化学方程式为
,所以F→G的化学方程式为 ,
,
故答案为: ;
;
(5) D的结构简式为 ,X是D的同系物,X分子比D分子少一个碳原子,且能发生银镜反应,说明X的分子中含有苯环且属于酯类,同时含有醛基,应为甲酸酯,苯环侧链共有3个碳原子,则满足此条件的X结构为:
,X是D的同系物,X分子比D分子少一个碳原子,且能发生银镜反应,说明X的分子中含有苯环且属于酯类,同时含有醛基,应为甲酸酯,苯环侧链共有3个碳原子,则满足此条件的X结构为:
苯环上有1个取代基的可能是:HCOOCH2CH2-和HCOOCH(CH3)-,2种;
苯环上有2个取代基的可能是:HCOO-和-CH2CH3,HCOO CH2-和-CH3,各有邻间对3种,共6种;
苯环上有3个取代基的:1个HCOO-和2个-CH3,共6种;总共14种;
其中核磁共振氢谱显示为5组峰,其峰面积比为3︰2︰2︰2︰1,符合该要求的X的同分异构体的结构简式为:  (或
(或 ),
),
故答案为: (或
(或 );
);
(6)根据Prolitane的合成路线,若要制备苯甲酸乙酯,应由苯甲酸和乙醇发生酯化反应来制备,可以设计以苯为原料制备溴苯,结合B转化为C的反应原理,由溴苯制取苯甲酸,具体合成路线为: ,
,
故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】氢能被视为最具发歸力的清洁能源,开发新型储氣材料是氢能利用的重要研究方向。请回答下列问题:
Ⅰ.化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=NH)3通过如 下反应制得:3CH4+2 (HB=NH) 3+6H2O=3CO2+6H3BNH3
(1)基态B原子的价电子排布式为___________,B、C, N, O第一电离能由大到小的顺序为_________,CH4、H2O、CO2的键角按照由大到小的顺序排列为___________。
(2)与(HB=NH)3,互为等电子体的有机分子为___________(填分子式)。
Ⅱ.氢气的安全贮存和运输是氢能应用的关键。
(1)印度尼赫鲁先进科学研宄中心的Datta和Pati等人借助ADF软件对一种新 型环烯类储氢材料(C16S8)进行研宄,从理论角度证明这种材料的分子呈平面结构(如图),每个杂环平面上下两侧最多可吸附10个H2分子。
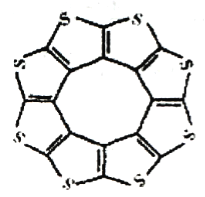
①C16S8分子中C原子和S原子的杂化轨道类型分别为___________。
②相关键长数据如表所示:
化学键 | C-S | C=S | C16S8中碳硫键 |
键长/pm | 181 | 155 | 176 |
从表中数据看出,C16S8中碳硫键键长介于C—S键与C=S键之间,原因可能______________________。
③C16S8与H2微粒间的作用力是___________。
(2)有储氢功能的铜合金晶体具有立方最密堆积结构,晶胞中Cu原子位于面心,Ag 原子位于顶点,氢原子可进到由Cu原子与Ag原子构成的四面体空隙中。该晶体储氢后的晶胞结构与CaF2(如图)相似,该晶体储氢后的化学式为___________。

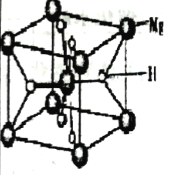
(3)MgH2是金属氢化物储氢材料,其晶胞如上图所示,该晶体的密度为agcm-3,则晶胞的体积为___________cm3(用含a、NA的代数式表示,NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 已知冰的熔化热为6.0kJ·mol-1,冰中氢键键能为20kJmol-1,假设每摩尔冰中有2mol氢键,且熔化热完全用于打破冰的氢键,则最多只能破坏冰中15%的氢键
B. 已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为a,Ka=(ca)2/c(1-a)。若加水稀释,,则CH3COOH![]() CH3COO-+H+向右移动,a增大,Ka不变
CH3COO-+H+向右移动,a增大,Ka不变
C. 甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3kJ·mol-1
D. 500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G均为常见的有机物,它们之间有如下转化关系。已知:①A是一种植物生长调节剂,有催熟作用;②醛基在氧气中易被氧化成羧基。回答下列问题: 
(1)A和B中官能团名称分别是___和___。
(2)在F的众多同系物中:最简单的同系物其空间构型为___;含5个碳原子的同系物其同分异构体有___种,其中一氯代物种类最少的同系物的结构简式为___。
(3)反应⑥和⑦均可得到G,要制备得到较纯净的G,应该选用反应_____。
(4)反应①﹣⑦属取代反应的有___;反应④中,浓硫酸的作用是___。反应②的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮和硫的化合物在工农业生产、生活中具有重要应用。请回答下列问题:
(1)航天领域中常用N2H4作为火箭发射的助燃剂。N2H4与氨气相似,是一种碱性气体,易溶于水,生成弱碱N2H4·H2O。用电离方程式表示N2H4·H2O显碱性的原因是:____________________________________________。
(2)在恒温条件下,1 mol NO2和足量C发生反应2NO2(g)+2C(s)![]() N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
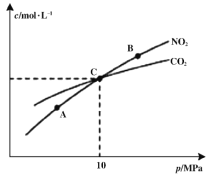
①A、B两点的浓度平衡常数关系:Kc(A) ___________Kc(B)(填“<”或“>”或“=”)
②A、B、C三点中NO2的转化率最高的是___________(填“A”或“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp=___________MPa(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)已知:亚硝酸(HNO2)性质和硝酸类似,但它是一种弱酸。常温下亚硝酸的电离平衡常数Ka=5.1×10-4;H2CO3的Ka1=4.2×10-7,Ka2=5.61×10-11。在常温下向含有2mol碳酸钠的溶液中加入1mol的HNO2后,则溶液中CO32-、HCO3-和NO2-的离子浓度由大到小的顺序是______________________。
(4)已知:常温下甲胺(CH3NH2)的电离常数为Kb,且pKb=-lgKb=3.4水溶液中有CH3NH2+H2OCH3NH3++OH-。常温下向CH3NH2溶液滴加稀硫酸至c(CH3NH2)=c(CH3NH3+)时,则溶液pH=_______。
(5)一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,但产生的CO又会与CaSO4发生化学反应,相关的热化学方程式如下:
①CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g) △H=+210.5kJ· mol-1
②CaSO4(s)+4CO(g) CaS(s)+ 4CO2(g) △H=-189.2 kJ· mol-1
反应CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g) △H=___________ kJ· mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国自主研发的“蓝鲸一号”在中国南海神狐海域完成可燃冰连续试采,并得到中共中央国务院公开致电祝贺。“可燃冰”是天然气水合物,外形像冰,在常温常压下迅速分解释放出甲烷,被称为未来新能源。
(1)“可燃冰”作为能源的优点是_______________________________(回答一条即可)。
(2)甲烷自热重整是一种先进的制氢方法,包含甲烷氧化和蒸汽重整两个过程。向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应如下:
反应过程 | 化学方程式 | 焓变△H(kJ.mol-l) | 活化能E.(kJ.mol-1) |
甲烷氧化 | CH4(g)+ | -802.6 | 125.6 |
CH4(g)+O2(g) | -322.0 | 172.5 | |
蒸气重整 | CH4(g)+H2O(g) | +206.2 | 240.1 |
CH4(g)+2H2O(g) | +158. 6 | 243.9 |
回答下列问题:
①在初始阶段,甲烷蒸汽重整的反应速率______(填“大于”“小于”或“等于”)甲烷氧化的反应速率。
②反应CH4(g)+H2O(g)![]() CO(g)+3H2(g)的平衡转化率与温度、压强关系[其中n(CH4):n(H2O)=1:1]如图所示。
CO(g)+3H2(g)的平衡转化率与温度、压强关系[其中n(CH4):n(H2O)=1:1]如图所示。
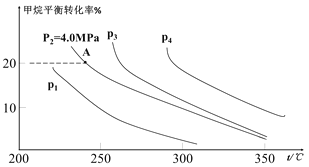
该反应在图中A点的平衡常数Kp=________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),图中压强(p1、p2、p3、p4)由大到小的顺序为___________。
③从能量角度分析,甲烷自热重整方法的先进之处在于___________。
(3)甲烷超干重整CO2技术可得到富含CO的气体,其能源和环境上的双重意义重大,甲烷超干重整CO2的催化转化原理如图所示。
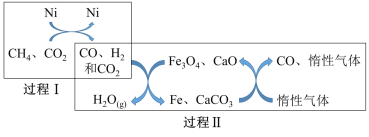
①过程II中第二步反应的化学方程式为_________。
②过程II的催化剂是______,只有过程I投料比![]() _______,催化剂组成才会保持不变。
_______,催化剂组成才会保持不变。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019 年是“国际化学元素周期表年”。 1869 年门捷列夫把当时已知的元素根据物理、化学性质进行排列,准确预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下。下列说法中错误的是

A. 甲位于现行元素周期表第四周期第ⅢA 族B. 原子半径比较:甲>乙> Si
C. 乙的简单气态氢化物的稳定性强于CH4D. 推测乙的单质可以用作半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应①2H2O(l)![]() 2H2(g)+O2(g)+Q1和反应②2H2O(l)
2H2(g)+O2(g)+Q1和反应②2H2O(l)![]() 2H2(g)+O2(g)+Q2,都是分解得到H2和O2,下列判断错误的是( )
2H2(g)+O2(g)+Q2,都是分解得到H2和O2,下列判断错误的是( )
A. 反应①中太阳能转化为化学能B. 反应②中电能转化为化学能
C. Q1>0、Q2<0D. Q1=Q2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组为了研究外界条件对化学反应速率的影响,进行了酸性高锰酸钾与草酸的反应,记录以下实验数据:
实验编号 | 实验温度 | 试管中所加试剂及其用量 / mL | 溶液褪至无色所需时间/ min | |||
0.6mol/L H2C2O4 溶液 | H2O | 3mol/L H2SO4 稀溶液 | 0.05mol/L KMnO4溶液 | |||
① | 25 | 3.0 | V1 | 2.0 | 3.0 | 1.5 |
② | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
③ | 50 | 2.0 | V2 | 2.0 | 3.0 | 1.0 |
(1)请写出该反应的离子方程式__________________________________________,当该反应以表中数据反应完全时转移电子数为_______________NA
(2)V1 ______
(3)根据上表中的实验①、②数据,可以得到的结论是_____。
(4)探究温度对化学反应速率的影响,应选择_____(填实验编号)
(5)该小组同学根据经验绘制了 n (Mn 2+ )随时间变化的趋势如图 1 所示,但有同学查阅已有的实验资料发现,该实验过程中 n (Mn 2+ ) 随时间变化的实际趋势如图 2 所示。
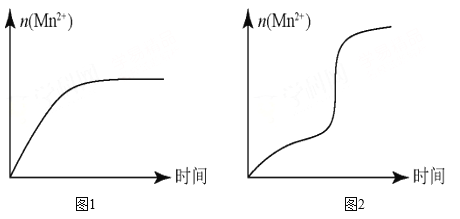
该小组同学根据图 2 所示信息提出了新的假设,并设计以下实验方案继续进行实验探究。
实验编号 | 实验温度/℃ | 试管中所加试剂及其用量 | 再加入某种固体 | 溶液褪至无色所需时间 / min | |||
④ | 25 | 0.6mol/L H2C2O4 溶液 | H2O | 3mol/L H2SO4 稀溶液 | 0.05mol/L KMnO4 溶液 | ||
2.0 | 3.0 | 2.0 | 3.0 | MnSO4 | t | ||
①该小组同学提出的假设是_____。
②若该小组同学提出的假设成立,应观察到_________________________________现象。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com