
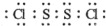 .
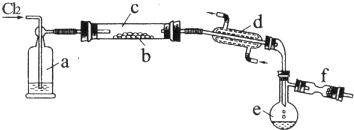
.分析 (1)根据仪器的形状确定名称;
(2)S2Cl2分子结构与H2O2相似,S2Cl2分子中氯原子与硫原子之间形成1对共用电子对,硫原子与硫原子之间形成1对共用电子对;
(3)由信息可知S2Cl2遇水水解,进入b中的气体应该干燥.硫的熔点较低,加热容易融化,防止熔融的硫堵塞导管.管.d为冷凝管,使生成的S2Cl2冷凝成液体;
(4)F装置盛放碱石灰,吸收Cl2尾气,防止空气中的水汽加入e中;
(5)只有硫元素化合价发生变化.
解答 解:(1)d为冷凝管,e为蒸馏烧瓶,故答案为:直形冷凝管(或冷凝管);蒸馏烧瓶;
(2)S2Cl2分子结构与H2O2相似,S2Cl2分子中氯原子与硫原子之间形成1对共用电子对,硫原子与硫原子之间形成1对共用电子对,S2Cl2电子式为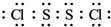 ,故答案为:
,故答案为: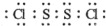 ;
;
(3)由信息可知S2Cl2遇水水解,进入b中的气体应该干燥.用浓硫酸干燥,a中应放试剂为浓硫酸,其作用为干燥氯气;
硫的熔点较低,加热容易融化,装置c水平放置防止熔融的硫堵塞导管,故答案为:浓H2SO4;防止熔融的硫堵塞导管;
(4)F装置盛放碱石灰,吸收Cl2尾气,防止污染环境,防止空气中的水汽加入e中使S2Cl2水解,故答案为:碱石灰;吸收Cl2尾气,并防止空气中的水汽使S2Cl2水解;
(5)只有硫元素化合价发生变化,且被氧化和被还原的物质的量之比为1:3,化学方程式:2S2Cl2+2H2O=SO2↑+3S↓+4HCl,故答案为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl.
点评 本题考查学生对实验原理及装置的理解、评价,阅读题目获取信息的能力等,关键是掌握整个制备流程原理,分析流程中各装置的作用,要求学生要有扎实的实验基础知识和灵活应用信息解决问题的能力,难度中等.


 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:多选题
| A. | 测0.01mol/L的醋酸的pH为5:CH3COOH?CH3COO-+H+ | |
| B. | 电解饱和食盐水,产生气体:2Cl-+2H2O$\frac{\underline{\;高温\;}}{\;}$Cl2↑+2OH-+H2↑ | |
| C. | 铁放在氧气中燃烧,产生黑色固体:4Fe+3O 2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | |
| D. | 硫酸钙与碳酸钠溶液,产生白色沉淀:CaSO4(S)+CO32-?CaCO3(S)+SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 元素X有三种同位素 | |
| B. | 其中一种同位素质量数为36 | |
| C. | 质量数为35的同位素原子的质量分数为75% | |
| D. | 元素单质X2的平均式量为71 |
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上学期第13次周测理科综合化学试卷 题型:选择题
我国晋代《抱朴子》中描述了大量的化学反应,其中有:①“丹砂(HgS)烧之成水银,积变又还成丹砂”; ②“以曾青涂铁,铁赤色如铜”。下列有关叙述正确的是
A.①中水银“积变又还成丹砂”说明水银发生了还原反应
B.②中反应的离子方程式为:2Fe+3Cu2+=2Fe3++3Cu
C.根据①可知温度计打破后可以用硫粉覆盖水银,防止中毒
D.水银能跟曾青发生置换反应生成单质铜
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 )与苯环性质相似.有机物M与磷酸在一定条件下形成磷酸吡醛,磷酸吡醛是细胞的重要组成部分.下列说法不正确的是( )
)与苯环性质相似.有机物M与磷酸在一定条件下形成磷酸吡醛,磷酸吡醛是细胞的重要组成部分.下列说法不正确的是( )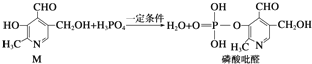
| A. | M能使酸性高锰酸钾溶液褪色 | |
| B. | 1 mol磷酸吡醛与足量的金属钠反应,最多消耗2mol Na | |
| C. | 1 mol磷酸吡醛与NaOH溶液反应,最多消耗4mol NaOH | |
| D. | M与足量H2反应后所得有机物的分子式为C8H17O3N |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,8 g O2与8 g O3均含有4 NA个电子 | |
| B. | 标准状况下,2.24 L SO3的分子数为0.1 NA | |
| C. | 1L 1mol•L-1盐酸中含有NA个HCl分子 | |
| D. | 0.1 mol Fe与足量浓HNO3反应,转移电子数为0.3 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com