
| A. | 原电池是把电能转变为化学能的装置 | |
| B. | 原电池中电子流出的一极是负极,发生氧化反应 | |
| C. | 原电池的两极发生的反应均为氧化还原反应 | |
| D. | 形成原电池后,原电池中的阳离子向负极方向移动 |
分析 将化学能转变为电能的装置是原电池,其电极材料是两种活泼性不同的金属或导电的非金属,负极上发生氧化反应,正极上发生还原反应,电子从负极流向正极,电流方向相反,以此解答该题.
解答 解:A.原电池是向外提供电能的装置,将化学能转变为电能,故A错误;
B.原电池的负极上失电子发生氧化反应,正极上得电子发生还原反应,电子由负极经外电路流向正极,故B正确;
C.正极发生还原反应,故C错误;
D.原电池工作时,阳离子向正极移动,故D错误.
故选B.
点评 本题考查原电池原理,为高频考点,题目难度不大,注意原电池的电极材料不一定都是金属,且不一定是较活泼的金属作负极,如镁、铝和氢氧化钠溶液构成的原电池中,铝作负极,为易错点.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
 苯乙烯是重要的基础有机原料.工业中用乙苯(C6 H5-CH2 CH3)为原料,采用催化脱氢的方法制取苯乙烯(C6 H5-CH=CH2)的反应方程式为:
苯乙烯是重要的基础有机原料.工业中用乙苯(C6 H5-CH2 CH3)为原料,采用催化脱氢的方法制取苯乙烯(C6 H5-CH=CH2)的反应方程式为: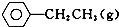 ?催化剂
?催化剂 ═CH2(g)+H2(g)
═CH2(g)+H2(g)| 化学键 | C-H | C-C | C=C | H-H |
| 键能/kJ/mol | 412 | 348 | 612 | 436 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100mL 1mol•L-1的NaCl溶液 | B. | 150mL 1mol•L-1的MgCl2溶液 | ||
| C. | 200mL 1mol•L-1的HCl溶液 | D. | 10mL 1mol•L-1的AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 46gNO2和N2O4混合气体中含有原子总数为3NA | |
| B. | 1molCl2与足量的铁反应,转移的电子数为2NA | |
| C. | 常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.2NA | |
| D. | 1 mol Na 与足量O2 反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在通常状况下,A为固态单质.根据下图转化关系,回答:
在通常状况下,A为固态单质.根据下图转化关系,回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②③ | B. | 只有③④ | C. | 都正确 | D. | 都错误 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
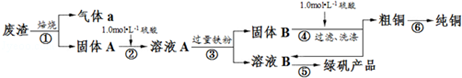

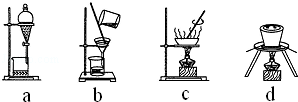
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.90 | 20.02 | 19.98 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
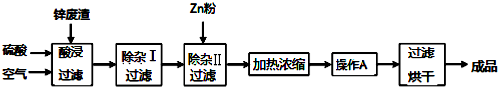
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 | Cu(OH)2 |
| 开始沉淀的 pH | 3.3 | 1.5 | 6.5 | 5.4 | 4.2 |
| 沉淀完全的 pH | 5.2 | 3.7 | 9.7 | 8.0 | 6.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com