
已知H2(g)+I2(g)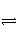
 2HI(g) ΔH<0。有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2 mol,相同温度下分别达到平衡浓度。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
2HI(g) ΔH<0。有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2 mol,相同温度下分别达到平衡浓度。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
A.甲、乙提高相同温度
B.甲中加入0.1 mol He,乙不变
C.甲降低温度,乙不变
D.甲增加0.1 mol H2,乙增加0.1 mol I2
科目:高中化学 来源: 题型:
如图装置中,小试管内为红墨水,具支试管内盛有pH=4久置的雨水和生铁片。实验时观察到:开始时导管内液面下降,一段时间后导管内液面回升,略高于小试管内液面。下列说 法正确的是( )
法正确的是( )
A.生铁片中的碳是原电池的阳极,发生还原反应
B.雨水酸性较强,生铁片仅发生析氢腐蚀
C.墨水回升时,碳电极反应式为O2+2H2O+4e-===4OH-
D.具支试管中溶液pH逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
以石墨为电极,电解KI溶液(其中含有少量酚酞和淀粉)。下列说法错误的是
A.阴极附远溶液呈红色 B.阴极逸出气体
C.阳极附近溶液呈蓝色 D.溶液的pH变小
查看答案和解析>>
科目:高中化学 来源: 题型:
今有甲、乙、丙三瓶等体积的新制氯水,浓度均为
0.1 mol· L-1。如果在甲中加入少量的碳酸氢钠晶体m mol,在乙中加入少量的亚硫酸氢钠晶体m mol,丙瓶不变,片刻后,甲乙丙三溶液中HClO的物质的量浓度大小关系是(溶液体积变化不计)( )
A.甲=乙>丙 B.甲>丙>乙
C.丙>甲=乙 D.乙>丙>甲
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z的原子序数依次增大,X和Y同主族,Y和Z同周期,Y与Z能形成离子个数比为1∶1的离子化合物A,X与Z能形成原子个数比为1∶1的共价化合物B,它们之间能实现如图所示转化(部分产物已略去):
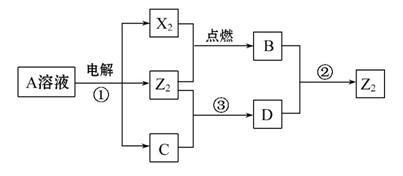
(1)Y在周期表的位置是 ;
(2)反应①的化学方程式是_______________ 。
(3)D溶液呈碱性的原因是(用离子方程式表示) _________________。
D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应。某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,仪器装置如图所示
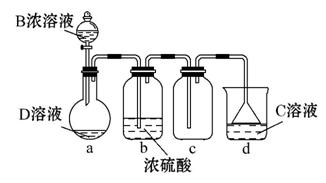
ⅰ.写出反应②的离子方程式___________ 。
ⅱ.上述实验装置不够完善,改进方法是 _____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一真空密闭容器中盛有1 mol PCl5,加热到200℃,发生反应:PCl5(g)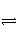
 PCl3(g)+Cl2(g),反应达到平衡时,PCl5在混合气体中的体积分数为m%,若在相同的温度和相同的容器中,起始时加入2 mol PCl5,反应达到平衡时,PCl5在混合气体中的体积分数为n%,则m和n的关系正确的是( )
PCl3(g)+Cl2(g),反应达到平衡时,PCl5在混合气体中的体积分数为m%,若在相同的温度和相同的容器中,起始时加入2 mol PCl5,反应达到平衡时,PCl5在混合气体中的体积分数为n%,则m和n的关系正确的是( )
A.m>n B.m<n C.m=n D.无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,4 mol A和5 mol B通入一个定容的密闭容器里,发生反应4A(g)+5B(g)
 6C(g),当此反应进行到一定程度时,达到平衡状态。现在该容器中,维持温度不变,令a、b、c分别代表初始加入的A、B、C的物质的量。如果a、b、c取不同的数值,它们必须满足一定的关系,才能保证达到平衡时,反应混合物中三种物质的质量分数仍跟上述平衡时完全相同,请填写下列空白:
6C(g),当此反应进行到一定程度时,达到平衡状态。现在该容器中,维持温度不变,令a、b、c分别代表初始加入的A、B、C的物质的量。如果a、b、c取不同的数值,它们必须满足一定的关系,才能保证达到平衡时,反应混合物中三种物质的质量分数仍跟上述平衡时完全相同,请填写下列空白:
(1)若a=0 mol,b=0 mol,则c=________。
(2)若a=1 mol,则b=________,c=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用4种溶液进行实验,下表中“操作及现
象”与“溶液”对应关系错误的是( )
| 选项 | 操作及现象 | 溶液 |
| A | 通入CO2,溶液变浑浊。再升高至65℃以上,溶液变澄清。 | C6H5ONa溶液 |
| B | 通入CO2,溶液变浑浊。继续通CO2至过量,浑浊消失。 | Na2SiO3溶液 |
| C | 通入CO2,溶液变浑浊。再加入品红溶液,红色褪去。 | Ca(ClO)2溶液 |
| D | 通入CO2,溶液变浑浊。继续通CO2至过量,浑浊消失,再加入足量NaOH溶液,又变浑浊 | Ca(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物Bilirubin在一定波长的光的照射下发生分解反应,反应物浓度随反应时间变化如下图所示,计算反应4~8 min间的平均反应速率和推测反应16 min时反应物的浓度,结果应是( )
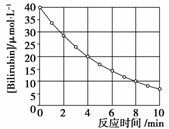
A.2.5 μmol·L-1·min-1和2.0 μmol·L-1
B.2.5 μmol·L-1·min-1和2.5 μmol·L-1
C.3.0 μmol·L-1·min-1和3.0 μmol·L-1
D.5.0 μmol·L-1·min-1和3.0 μmol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com