
���п�ͼ�е����ʾ�Ϊ��ѧ��ѧ�г������ʣ����мס���Ϊ���ʣ������Ϊ�����BΪ����Һ̬�����AΪ����ɫ���壬F��G����Ԫ����ͬ�Ҿ�Ϊ�Ȼ��G��KSCN��Һ�Ժ�ɫ��
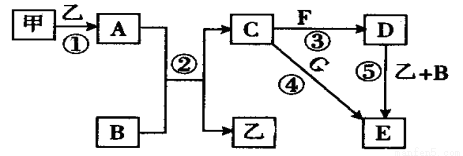
��ش��������⣺
��1��A B�� C�� D�� E��
��2����Ӧ��~���У�����������ԭ��Ӧ���� ������ţ���
��3����Ӧ�ݵĻ�ѧ����ʽΪ ��
����B��Ӧ�����ӷ���ʽΪ ��
A��B��Ӧ�����ӷ���ʽΪ ��
��4���ڿ����н�C��Һ����F��Һ�У��۲쵽�������� ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�����ʡ������ѧ��9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ĩX�п��ܺ���Fe��FeO��CuO��MnO2��KCl��K2CO3�е������֡�Ϊȷ���ù����ĩ�ijɷ֣�ijͬѧ���ν���������ʵ�飺
�ٽ�X��������ˮ�У��õ�������Y����ҺZ��
��ȡ����Y��������Ũ���ᣬ���ȣ���������ɫ���壬����������ɫ�����
����Z��Һ�еμ�AgNO3��Һ�����ɰ�ɫ������
���ò�����պȡ��ҺZ�ڹ㷶pH��ֽ�ϣ���ֽ����ɫ��
��������ʵ���������н�����ȷ���ǣ� ��
A��X��һ��������FeO B��������Y��һ������Fe��CuO
C��Z��Һ��һ������KCl��K2CO3 D��Y�в�һ������MnO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���㽭ʡ�����и�����ѧ����Ӧ�Կ��Ի�ѧ�Ծ��������棩 ���ͣ�������
�ձ���ʢ��NaHSO4��Na2SO4�����Һ���Ϊ100mL�����ձ�����μ���0.15mol��L-1 Ba(OH)2��Һ�����������ﵽ���ֵʱ����Һ�������Ϊ200mL����Һ�в������������ʵ���n����Һ��pH�仯��ͼ��ʾ��

��ش�
��1��ԭ��Һ��c(NaHSO4)= mol��L-1��
��2��ͼ��aֵΪ mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���㽭ʡ�����и�����ѧ����Ӧ�Կ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���淴Ӧ��һ�������´ﵽ��ѧƽ��ʱ������˵����ȷ���ǣ� ��
A������Ӧ���ʵ����淴Ӧ���ʣ��Ҷ�Ϊ��
B����Ӧ���������Ũ�����
C����Ӧ��ϵ�л�������ɱ��ֲ���
D���Ͽ���ѧ�����յ����������γɻ�ѧ�����ų�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���㽭ʡ�����и�����ѧ����Ӧ�Կ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʵ�ˮ��Һ��ˮ��������Ե��ǣ� ��
A��HCl B��NH4Cl C��Na2CO3 D��NaCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���Ĵ�ʡ�����и�����ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�δ�������ҽѧ���δȵġ�ϴԩ��¼�����������鶾�ļ��أ��������鶾���漰�Ļ�ѧ��Ӧ�� 4Ag + 2H2S + O2 �� 2X + 2H2O������˵����ȷ���ǣ� ��
A��X�Ļ�ѧʽΪAgS
B�������鶾ʱ������������ʧȥ����
C����Ӧ��Ag��H2S���ǻ�ԭ��
D��ÿ����1mo1X����Ӧת��2mo1 ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��ɽ��ʡ�����и�����ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ������
�״���һ�ֿ�������Դ�����п�����Ӧ�õĹ���ǰ������ҵ��һ��ɲ������·�Ӧ���ϳɼ״��� CO(g)+2H2(g)  CH3OH(g)������ʵ����ģ��÷�Ӧ�����з�����
CH3OH(g)������ʵ����ģ��÷�Ӧ�����з�����
��1�����и����У����ܹ�˵���÷�Ӧ�Ѵﵽƽ�����__________������ţ���
a�����¡����������£������ڵ�ѹǿ�������仯
b��һ�������£�CH3OH�ֽ�����ʺ�CH3OH���ɵ��������
c��һ�������£�CO��H2��CH3OH��Ũ�ȱ��ֲ���
d��һ�������£���λʱ��������2 mol CO��ͬʱ����1 mol CH3OH
��2����ͼ�Ǹ÷�Ӧ�ڲ�ͬ�¶���CO��ת������ʱ��仯�����ߡ�

�� �÷�Ӧ���ʱ䦤H____________0(�����������������)��
�� T1��T2�¶��µ�ƽ�ⳣ����С��ϵ��K1____________K2(�����������������)��
�� �������ݻ����䣬���д�ʩ�����Ӽ״����ʵ���______________��
a�������¶�
b����CH3OH(g)����ϵ�з���
c��ʹ�ú��ʵĴ���
d������He��ʹ��ϵ��ѹǿ����
��3��2009��10�£��й���ѧԺ����Ӧ�û�ѧ�о����ڼ״�ȼ�ϵ�ؼ�����������ͻ�ƣ��״�ȼ�ϵ�صĹ���ԭ������ͼ��ʾ��

����д��c��ͨ������ʷ�������Ӧ�缫��Ӧʽ_________
�ڹ���һ��ʱ���0.2 mol�״���ȫ��Ӧ����CO2 ʱ����___________������ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��ɽ��ʡ�����и�����ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����ͭƬ�϶���ʱ������������ȷ���ǣ� ��
�ٽ�ͭƬ���ڵ�Դ��������
�ڽ���Ƭ���ڵ�Դ��������
����ͭ�Ϸ����ķ�Ӧ�ǣ�Ag��+e�� �� Ag
������Ƭ�Ϸ����ķ�Ӧ�ǣ�4OH����4e�� �� O2��+2H2O
����������ͭ��ҺΪ���Һ
��������������ҺΪ���Һ
A���٢ۢ� B���ڢۢ� C���٢ܢ� D���ڢۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ������9���¿���ѧ�Ծ��������棩 ���ͣ������
һ���¶��£������������Ϊ2L�ĺ����ܱ������з�����Ӧ��
2CH3OH(g) CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)

�ش��������⣺
��1����Ӧ�ġ�H_________O ����������������жϵ�������_____________������I����ƽ�������ʱ��Ϊ20s����Ӧ����v(CH3OH)Ϊ_________mol/(L��s)��390��ʱ�÷�Ӧ��ƽ�ⳣ��K1=________������ֵ����
��2������II��ƽ��ʱ��ѹǿ������I��������CH3OH���������������I�е���ͬ��CH3OH��ʼ�����ʵ���Ϊ__________��ƽ��ʱCH3OH(g)���������Ϊ___________��
��3��t���Ӻ�����III�ﵽƽ�⣬t_________20s���>����<����=�������жϵ�������________��
������ͼ�зֱ�����I������III��CH3OH(g)Ũ�ȱ仯������ʾ��ͼ��

��4��390�棬����3L�����г���0.9mol CH3OH(g), 0.6mol CH3OCH3(g)��0.3molH2O(g)������ʼʱ�÷�Ӧ����V��_________V�档���>����<����=����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com