
分析 由实验流程淀粉液$→_{①△}^{试剂1}$水解液$→_{②}^{试剂2}$混合液$→_{③△}^{试剂3}$砖红色沉淀可知,试剂1为稀硫酸,稀硫酸为淀粉水解的催化剂,试剂2为NaOH,NaOH中和酸,反应③在碱性条件下发生,试剂3为新制的氢氧化铜悬浊液,若该实验中没有加碱至碱性,不能检验水解产物葡萄糖,结合淀粉遇碘单质变蓝判断水解程度,以此来解答.
解答 解:由实验流程淀粉液$→_{①△}^{试剂1}$水解液$→_{②}^{试剂2}$混合液$→_{③△}^{试剂3}$砖红色沉淀可知,试剂1为稀硫酸,试剂2为NaOH,反应③在碱性条件下发生,试剂3为新制的氢氧化铜悬浊液,(1)由上述分析可知,试剂1是稀硫酸,作用是起催化作用,
故答案为:稀硫酸;起催化作用;
(2)试剂2是NaOH溶液,作用是中和硫酸,
故答案为:NaOH溶液; 中和硫酸;
(3)如果实验过程中没有加入试剂2而直接加入试剂3,不能实现实验目的,其原因是硫酸能溶解Cu(OH)2而使实验失败,
故答案为:否;硫酸能溶解Cu(OH)2而使实验失败;
(4)检验第①步实验已基本完成的操作方法为用试管取出少量水解液,加入碘水,若不显蓝色,说明水解反应已基本完成,
故答案为:用试管取出少量水解液,加入碘水,若不显蓝色,说明水解反应已基本完成.
点评 本题考查有机物的性质实验,为高频考点,把握有机物的性质、实验技能等为解答的关键,侧重分析与实验能力的考查,注意淀粉、葡萄糖的性质及检验,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
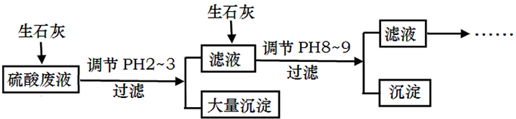
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
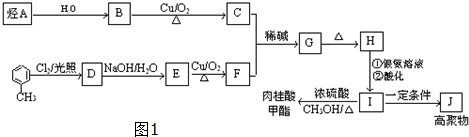
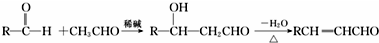
 $→_{△}^{硫酸}$
$→_{△}^{硫酸}$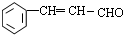 +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在酒精灯加热条件下,Na2CO3、NaHCO3固定都能发生分解 | |
| B. | 不可用元素周期律解释热稳定性:Na2CO3>NaHCO3 | |
| C. | 分别加热Na2CO3和NaHCO3固体,试管内壁均有水珠,则两种物质均受热分解 | |
| D. | 1L0.1mol•L-1NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠-钾合金可在核反应堆中用作热交换液 | |
| B. | 过氧化钠可用作潜水艇中的供氧剂 | |
| C. | 纯碱可用作治疗胃酸过多的药剂 | |
| D. | 碳酸氢钠溶液用于制泡沫灭火剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①③⑤ | B. | ①② | C. | ②③⑤ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在蒸发食盐水时,边加热边用玻璃棒搅拌直至液体蒸干 | |
| B. | 鉴别Na2CO3与NaHCO3固体可用加热的方法 | |
| C. | 实验室制备氢氧化铁胶体时,向饱和氯化铁溶液中滴加氢氧化钠溶液 | |
| D. | 配制一定物质的量浓度的NaOH溶液,将NaOH固体放在容量瓶中加水溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com