
| A、能使酚酞变红的溶液中:Ba2+、Br-、AlO2-、ClO- |
| B、与铁反应能够产生H2的溶液中:Na+、Mg2+、NO3-、Cl- |
| C、PH=0 的溶液中:Fe3+、Al3+、HS-、SO42- |
| D、由水电离产生的C(H+)=1×10-12 mol/L的溶液:NH4+、Na+、NO3-、Cl- |


科目:高中化学 来源: 题型:
| A、金属钠具有强还原性,可用与TiCl4溶液反应制取金属Ti |
B、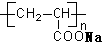 表示一种吸水性高分子树脂 表示一种吸水性高分子树脂 |
| C、用于现代建筑的钢筋混凝土不属于复合材料 |
| D、山东东营广饶县一男子收到网购物品后,因吸入氟乙酸甲酯中毒身亡,氟乙酸甲酯的结构简式为FCH2COOCH3,能与H2发生加成反应,也能被LiAlH4还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、60s内X的平均反应速率为0.001 mol?L-1?s-1 |
| B、将容器的容积变为20L,达平衡后Z的浓度为0.015 mol?L-1 |
| C、若温度和体积不变,往容器内增加1mol X,Y的转化率将增大 |
| D、若升高温度,X的体积分数增大,则正反应的△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
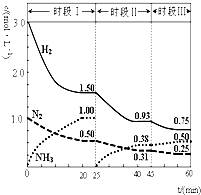 N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1.恒容时,体系中各物质浓度随时间变化的曲线如图示.下列说法不正确的是( )
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1.恒容时,体系中各物质浓度随时间变化的曲线如图示.下列说法不正确的是( )| A、前20分钟反应内放出的热量为46.2kJ |
| B、第25分钟改变的条件是将NH3从反应体系中分离出去 |
| C、若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度 |
| D、时段Ⅰ仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、OH-、AlO2-、S2- |
| B、K+、H+、Br-、HCO3- |
| C、Ba2+、Al3+、Cl-、SiO32- |
| D、K+、Fe3+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用托盘天平称取3.25gNaOH |
| B、将2 mol KCl溶于适量水中,配成1L溶液,所得溶液的物质的量浓度为2 mol/L |
| C、用10mL量筒量取6.45mL浓硫酸 |
| D、当温度高于0℃时,气体摩尔体积一定大于22.4L/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、自然界中含有大量的游离态的硅,纯净的硅晶体可用于制作计算机芯片 |
| B、Si、P、S、Cl相应的最高价氧化物对应水化物的酸性依次增强 |
| C、工业上通常用电解钠、铁、铜对应的氯化物制得该三种金属单质 |
| D、金属铝、铁、铜都有一定的抗腐蚀性能,其抗腐蚀的原因都是表面形成氧化物薄膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4CuO(s)═2Cu2O(s)+O2(g)在室温下不能自发进行,说明该反应△H>0 |
| B、向稀醋酸中加入醋酸钠固体,溶液pH升高的主要原因是醋酸钠水解呈碱性 |
| C、室温下K(HCN)<K(CH3COOH),说明CH3COOH的电离度一定比HCN大 |
| D、H2S(g)+FeO(s)?FeS(s)+H2O(g),其他条件不变时增大压强,反应速率V正(H2S)和H2S的平衡转化率均增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com