
分析 (1)根据表中数据可知硫酸溶液中不存在H2SO4,存在HSO4-,说明硫酸的第一步电离为完全电离,第二步电离为部分电离,据此写出电离方程式;
(2)向该溶液中加入过量氨水,反应生成硫酸铵,注意硫酸的第二步电离存在电离平衡;
(3)硫酸第一步完全电离,第二步部分电离,根据硫酸的浓度和HSO4-的电离度计算溶液中氢离子浓度,溶液中离子积常数计算氢氧根离子浓度;
(4)0.1mol/L的H2SO4溶液10.00mL和氨气反应恰好中和反应生成硫酸铵和水,结合反应定量关系计算氨气物质的量,得到标准状况下体积;
(5)向该溶液中加入1mol/L的氢氧化钡溶液,使溶液反应后的pH为13,溶液显碱性,计算剩余氢氧根离子浓度得到溶液体积.
解答 解:(1)根据表中数据可知硫酸溶液中不存在H2SO4,存在HSO4-,说明硫酸的第一步电离为完全电离,电离方程为:H2SO4=HSO4-+H+,第二步电离为部分电离,电离方程式为:HSO4-?H++SO42-;
故答案为:H2SO4=HSO4-+H+,HSO4-?H++SO42-;
(2)向该溶液中加入过量氨水,硫酸氢根离子存在电离平衡,一水合氨为弱电解质,反应生成硫酸铵,反应的离子方程式为:HSO4-+H++2NH3•H2O=2NH4++SO42-+2H2O,
故答案为:HSO4-+H++2NH3•H2O=2NH4++SO42-+2H2O;
(3)0.1mol•L-1稀硫酸中,硫酸第一步完全电离,电离出来的氢离子为0.1mol/L,第二步部分电离,电离的H+物质的量浓度=0.1mol/L×10%=0.01mol/L,所以两步共电离氢离子为0.11mol/L,离子积常数计算得到氢氧根离子浓度c(OH-)=$\frac{1{0}^{-14}}{0.11}$=9.09×10-12mol/L,
故答案为:9.09×10-12;
(4)0.1mol/L的H2SO4溶液10.00mL和,物质的量=0.1mol/L×0.010L=0.001mol,氨气反应恰好中和反应生成硫酸铵和水,H2SO4+2NH3+2H2O=(NH4)2SO4+2H2O,
需要氨气物质的量0.002mol,标准状况下气体体积=0.002mol×22.4L/mol=0.0448L=44.8ml,
故答案为:44.8;
(5)向0.1mol/L的H2SO4溶液中加入1mol/L的氢氧化钡溶液,使溶液反应后的pH为13,设硫酸溶液体积为x,氢氧化钡溶液体积为y,
$\frac{1mol/L×y×2-0.1mol/L×x×2}{(x+y)L}$=$\frac{1{0}^{-14}}{1{0}^{-13}}$
x:y=19:3,
则参加反应的硫酸溶液和氢氧化钡溶液的体积之比为19:3.
故答案为:19:3.
点评 本题考查了二元酸的电离方程式、离子浓度的求算、盐的水解规律的应用、离子浓度的比较、电离平衡常数的计算等,题目涉及的知识点较多,侧重反应原理的应用的考查,题目难度中等.


 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:推断题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.2gCH3OH含有的化学键数为0.4NA | |
| B. | 0.1molFeCl3水解制得的Fe(OH)3胶体中胶粒数是0.1NA | |
| C. | 标准状况下,2.24LCl2溶于足量水,转移的电子数为0.1NA | |
| D. | 0.2gD216O中含有的质子数、中子数和电子数均为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=$\frac{PM}{2000ρ}$ | B. | P=$\frac{200ρa}{M}$ | C. | P$\frac{1000ρ×a%}{M}$×2 | D. | V×ρ×a%=$\frac{PMV}{1000}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3和NaHCO3粉末与同浓度的盐酸时,Na2CO3因为碱性强,所以与盐酸反应放出气体速度快 | |
| B. | 等物质的量的两种盐与同浓度的盐酸反应,Na2CO3所消耗盐酸的体积是 NaHCO3的两倍 | |
| C. | 向Na2CO3饱和溶液中通人过量CO2,有NaHCO3结晶析出 | |
| D. | Na2CO3和NaHCO3溶液分别和BaCl2溶液反应,现象不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
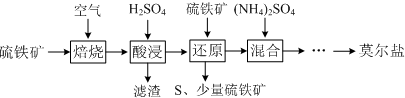
| 离子 | 离子浓度(mol•L-1) | |
| 还原前 | 还原后 | |
| SO42- | 3.20 | 3.50 |
| Fe2+ | 0.15 | 3.30 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 阳离子 | Na+ Mg2+ Al3+ Ba2+ Fe3+ |
| 阴离子 | OH- Cl- CO32- SO42- HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com