
【题目】把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中后有0.58克白色沉淀,在所得浊液中,逐滴加入0.5mol/L的盐酸,加入盐酸的体积与生成沉淀的质量关系如图所示:
(1)混合物中NaOH的物质的量为 ,
(2)混合物中AlCl3质量为 ,
(3)混合物中MgCl2质量为 ,
(4)P点表示盐酸的体积是 .
【答案】0.045mol;0.6675g;0.95g;90mL
【解析】(1﹣3)从图中可以看出,Mg(OH)2的质量为0.58 g,即0.01 mol,根据反应:MgCl2+2NaOH═2NaCl+Mg(OH)2↓,
m(MgCl2)=0.01 mol×95 gmol﹣1=0.95 g,n1(NaOH)=2n[Mg(OH)2]=0.02 mol.
开始至加入10 mL盐酸,发生反应:NaOH+HCl═NaCl+H2O,
n2(NaOH)=n(HCl)=0.5 molL﹣1×10×10﹣3L=5×10﹣3 mol.
盐酸的加入量从10~20 mL 发生反应:NaAlO2+HCl+H2O═Al(OH)3↓+NaCl,
n(NaAlO2)=n(HCl)=0.5 molL﹣1×(20﹣10)×10﹣3L=0.005 mol.
根据反应:AlCl3+4NaOH═NaAlO2+3NaCl+2H2O
n3(NaOH)=4n(NaAlO2)=0.02 mol,
m(AlCl3)=0.005 mol×133.5 gmol﹣1=0.6675g,
n(NaOH)=0.02 mol+5×10﹣3mol+0.02 mol=0.045mol.
故答案:(1)0.045mol;(2)0.6675g;(3)0.95g;
(2)根据反应:Al(OH)3+3HCl═AlCl3+3H2O,
Mg(OH)2+2HCl═MgCl2+2H2O
n(HCl)=0.005 mol×3+0.01 mol×2=0.035 mol
V(HCl)=![]() =70mL
=70mL
P点加入盐酸的体积为20mL+70mL=90mL.
答:P点所表示的盐酸的体积是90mL.


科目:高中化学 来源: 题型:
【题目】常温下向20mL0.1mol/LHA溶液中逐滴加入0.1mol/LNaOH溶液,其pH变化情况如图所示(忽略温度变化).下列说法中不正确的是( ) 
A.由题可知HA为弱酸
B.滴定终点位于c和d点之间
C.滴定到b点时:n(Na+)+n(H+)﹣n(OH﹣)+n(HA)=0.002mol
D.滴定到d点时:c(OH﹣)>c(Na+)>c(A﹣)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图示意铝在氧气中燃烧的实验,铝条点燃后,为维持燃烧继续,正确的操作是( ) 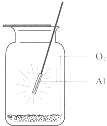
A.铝条应始终置于集气瓶瓶口位置
B.迅速将铝条插入集气瓶接近瓶底位置
C.将铝条从瓶口位置慢慢伸向瓶底位置
D.铝条应不断上下移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语中,正确的是( )
A. 次氯酸的结构式:H—O—Cl
B. 氮气的电子式:∶N∶∶∶N∶
C. CO2分子的电子式:O=C=O
D. 用电子式表示氯化氢分子的形成过程:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铝土矿中主要含有Al2O3、Al(OH)3、AlO(OH),还含有Fe2O3等杂质.利用拜耳法生产氧化铝的流程如图所示: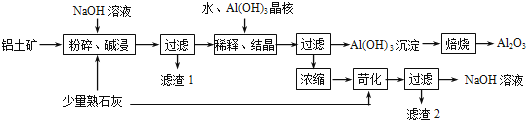
(1)粉碎后的铝土矿碱浸时应在高温下进行,其目的是 .
(2)AlO(OH)与NaOH反应的化学方程式为 .
(3)在稀释、结晶过程中:稀释的目的是 ;加Al(OH)3晶核的目的是促进Al(OH)3的析出.上述“稀释、结晶”工艺,也可用通入足量的 气体的方法来代替.
(4)浓缩所得的NaOH溶液由于吸收了空气中的CO2而含有杂质,该杂质可通过苛化反应除去,写出苛化反应的化学方程式: .
(5)该生产流程能实现 (填化学式)的循环利用.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在硫酸钠和硫酸铝的混合溶液中,Al3+的物质的量浓度为0.2mol·L-1,SO42-为0.4mol·L-1,溶液中Na+的物质的量浓度为( )
A. 0.1 mol·L-1B. 0.2mol·L-1C. 0.3mol·L-1D. 0.4mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com