
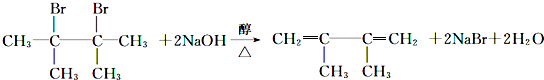 .
.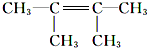 ;F1的结构简式是
;F1的结构简式是 .
.分析 烷烃A与氯气发生取代反应生成卤代烃B,B发生消去反应生成C1、C2,C1与溴发生加成反应生成二溴代物D,D再发生消去反应生成E,E与溴可以发生1,2-加成或1,4-加成,故C1为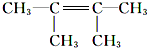 (CH3)2C=C(CH3)2,C2为
(CH3)2C=C(CH3)2,C2为 ,则D为
,则D为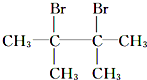 ,E为
,E为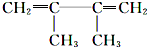 ,F1为
,F1为 ,F2为
,F2为 ,以此来解答.
,以此来解答.
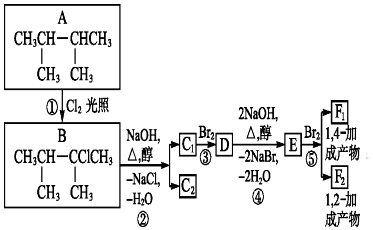
解答 解:(1)A中含6个C、14个H,分子式为C6H14,由结构可知,4个甲基相同、2个次甲基相同,含2种H,A的核磁共振氢谱有2组峰,其峰面积之比为12:2=6:1,根据系统命名法可知主链含4个C,2、3号C上有甲基,化合物A的名称是:2,3-二甲基丁烷,
故答案为:C6H14;2;6:1;2,3-二甲基丁烷;
(2)上述反应中,反应①中A中H原子被Cl原子确定生成B,属于取代反应,反应③是碳碳双键与溴发生加成反应是,
故答案为:取代;加成;
(3)由D生成E是卤代烃发生消去反应,该反应的化学方程式为: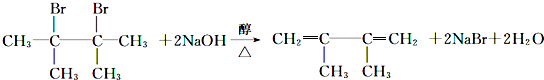 ,
,
故答案为: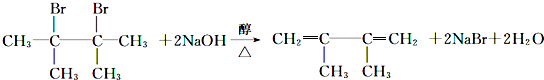 ;
;
(4)由上述分析可知C1的结构简式是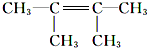 ,F1的结构简式是
,F1的结构简式是 ,
,
故答案为: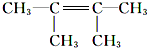 ;
; ;
;
(5)上述8种化合物中,属于二烯烃的是E,含2个碳碳双键,故答案为:E;
(6)E为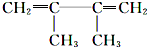 ,只含有一个碳碳三键的E的同分异构体骨架有C≡C-C-C-C-C、C-C≡C-C-C-C、C-C-C≡C-C-C、C≡C-C(CH3)-C-C、C≡C-C-C(CH3)-C、C≡C-C(CH3)3、C-C≡C-C(CH3)-C,共7种,故答案为:7.
,只含有一个碳碳三键的E的同分异构体骨架有C≡C-C-C-C-C、C-C≡C-C-C-C、C-C-C≡C-C-C、C≡C-C(CH3)-C-C、C≡C-C-C(CH3)-C、C≡C-C(CH3)3、C-C≡C-C(CH3)-C,共7种,故答案为:7.
点评 本题考查有机物的推断,为高频考点,把握官能团与性质、碳链变化、官能团的变化、有机反应为解答的关键,侧重分析与推断能力的考查,注意二烯烃及同分异构体的判断,题目难度中等.


科目:高中化学 来源: 题型:选择题
 短周期元素W、X、Y、Z的原子序数依次增加.甲为元素Z的单质,通常为淡黄色固体,乙、丙、丁、戊为这些元素组成的化合物,常温下0.1mol•L-1乙溶液pH为13,戊为Z的最高价氧化物的水化物.上述物质间的转化关系如图所示(部分产物及反应条件已略去).下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.甲为元素Z的单质,通常为淡黄色固体,乙、丙、丁、戊为这些元素组成的化合物,常温下0.1mol•L-1乙溶液pH为13,戊为Z的最高价氧化物的水化物.上述物质间的转化关系如图所示(部分产物及反应条件已略去).下列说法正确的是( )| A. | 简单离子的半径大小X<Y<Z | |
| B. | 化合物乙中含离子键和非极性共价键 | |
| C. | W与Z形成的化合物常温常压下呈液态 | |
| D. | 图中生成甲的离子方程式为6H++SO32-+2S2-=3S↓+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH2CH3与CH3CH(CH3)2 | B. | CH3CH═C(CH3)2与CH2═CHCH(CH3)2 | ||
| C. |  与 与 | D. |  与 与 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 海洋中有丰富的食品、矿产、能源、药物和水产资源,如图为海水利用的部分过程.下列有关说法正确的是( )
海洋中有丰富的食品、矿产、能源、药物和水产资源,如图为海水利用的部分过程.下列有关说法正确的是( )| A. | 在第③、④、⑤步骤中,溴元素均被氧化 | |
| B. | 用澄清石灰水可鉴别NaHCO3和Na2CO3 | |
| C. | 制取NaHCO3的反应是利用其溶解度相对较小 | |
| D. | 工业上通过电解饱和MgCl2溶液制取金属镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 打开啤酒盖,立即有气体逸出 | |
| B. | 新制的氯水在光照条件下颜色变浅 | |
| C. | NO2和N2O4的混合体系,压缩容器体积,颜色变深 | |
| D. | 工业生产硫酸的过程中使用过量的O2,以提高SO2的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氢氧燃料电池是符合绿色化学理念的新型发电装置.下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石英只能用于生产玻璃 | |
| B. | 从海水提取物质不一定要通过化学反应才能实现 | |
| C. | 二氧化硅能与氢氧化钠溶液反应,故常用氢氧化钠溶液作为雕刻玻璃的试剂 | |
| D. | 为了提高土壤肥力,往往将碳铵与熟石灰混合使用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com