
| 物质 | H2(g) | A2(g) | B2(g) | HA(g) | HB(g) |
| 能量(kJ) | 436 | a | 193 | 432 | 366 |
| A. | 能量最高的分子是H2 | B. | 最稳定的分子是B2 | ||
| C. | a=243 | D. | HB(g)+A2(g)═B2(g)+HA(g) 是吸热反应 |
分析 A2(g)与氢气化合生成1molHA(g)时放出的热量为92.5kJ,可知$\frac{1}{2}$×a+$\frac{1}{2}$×436-432=-92.5,a=243,一般来说,物质的键能越大,越稳定,物质的内能越大,越不稳定,以此解答该题.
解答 解:A.氢气的键能较大,较稳定,则能量较HA、HB等低,故A错误;
B.B2的键能较小,较不稳定,故B错误;
C.A2(g)与氢气化合生成1molHA(g)时放出的热量为92.5kJ,可知$\frac{1}{2}$×a+$\frac{1}{2}$×436-432=-92.5,a=243,故C正确;
D.由表中数据可知,HB(g)+A2(g)═B2(g)+HA(g) 的反应热为(366+243)-(193+432)=-16,为放热反应,故D错误.
故选C.
点评 本题考查化学反应与能量的变化,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握反应热的计算、比较方法,难度不大.


科目:高中化学 来源: 题型:解答题
 晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞.NaCl晶体结构如图所示.
晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞.NaCl晶体结构如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na2O2+2H2O=4NaOH+O2↑ | B. | 2F2+2H2O=4HF+O2 | ||
| C. | 3NO2+H2O=NO+2HNO3 | D. | 3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$4H2+Fe3O4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
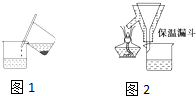
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
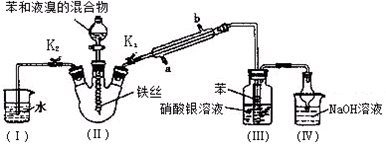
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
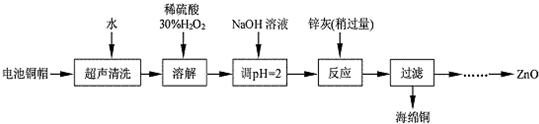
| 实验编号 | 1 | 2 | 3 | 4 |
| V(Na2S2O3)(mL) | 28.32 | 25.31 | 25.30 | 25.32 |
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 1.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
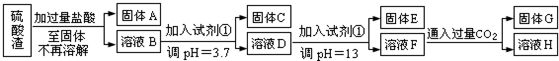

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com