
| A.由乙酸制备乙酸乙酯 |
| B.由碳制备饱和碳酸氢钠溶液 |
| C.证明氯的非金属性比硫强 |
| D.证明酸性:硫酸>碳酸>硅酸 |
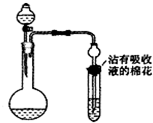
| 浓硫酸 |
| 加热 |


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源:2013届黑龙江省大庆市第三十五中学高三上学期期末考试化学试卷(带解析) 题型:实验题
(15分)某化学研究小组为测定Na2O2样品(仅含Na2O杂质)的纯度,设计了两种实验方案进行探究。
[实验一]取样品0.100 g,用右图所示实验装置进行测定。(夹持装置省略)
(1)检查装置A气密性的方法是 。
(2)若在实验过程中共产生气体11.20 mL(已折算成标准状况),则样品中Na2O2的纯度为 。
[实验二]样品溶于水后用盐酸滴定
(3)取一定量样品溶于水并稀释至250 mL,配制时,所用到的玻璃仪器除了烧杯和玻璃棒外,还需用到 。
(4)取上述所配溶液各25.00 mL,用一定浓度的标准盐酸滴定,平行实验记录如下表:
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 标准盐酸体积(mL) | 23.00 | 24.98 | 25.00 | 25.02 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
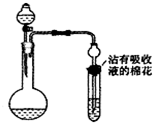 仅由右图装置(夹持和加热装置略去),难以完成的实验是
仅由右图装置(夹持和加热装置略去),难以完成的实验是查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
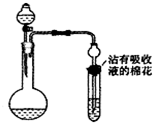
| A.由乙酸制备乙酸乙酯 |
| B.由碳制备饱和碳酸氢钠溶液 |
| C.证明氯的非金属性比硫强 |
| D.证明酸性:硫酸>碳酸>硅酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com