
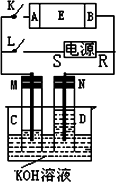
现有如图所示的装置,其中E为蘸有Na2SO4溶液(滴加酚酞)的滤纸,滤纸两端分别压有A、B铂片.R、S为电源的两电极,K、L为开关,M、N为多孔石墨电极.烧杯中盛有KOH浓溶液.将C、D玻璃管装满KOH浓溶液后倒置于烧杯中,接通开关K、L,通电一段时间后,C、D玻璃管中均有气体产生.
请回答:
(1)S为________极,B为________极.
(2)A极附近溶液的现象是____________.
N电极上发生的电极反应式为________.
(3)当玻璃管C、D中的气体产生到一定量时,切断开关L(K仍接通),在滤纸E的中间滴一滴紫色的KMnO4溶液,滤纸上的紫色点会移向________(填“A”或“B”)极.
科目:高中化学 来源: 题型:
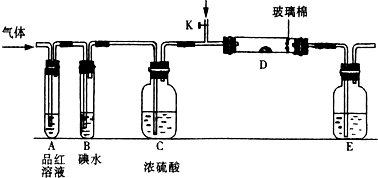
| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
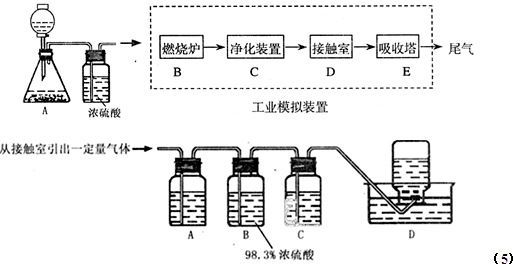
| ||
| ||
| ||
| ||
| 压强/Mpa 转化率 温度/℃ |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
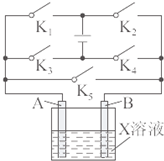 某课外活动小组准备用如图所示的装置进行实验.现有甲、乙、丙三位同学分别选择了如下电极材料和电解质溶液:
某课外活动小组准备用如图所示的装置进行实验.现有甲、乙、丙三位同学分别选择了如下电极材料和电解质溶液:| A电极 | B电极 | X溶液 | |
| 甲 | Cu | Zn | H2SO4 |
| 乙 | Pt | Pt | CuCl2 |
| 丙 | Fe | Cu | ? |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:高一化学 第3章 有机化合物的获得与应用 3.1.1 天然气的利用 甲烷(苏教版必修2) 苏教版 题型:058
实验室制CH4是用无水醋酸钠和碱石灰固体共热制取,其方程式为:H3COONa+NaOH![]() Na2CO3+CH4↑.回答:
Na2CO3+CH4↑.回答:
(1)实验室制取下列气体时,气体发生装置与实验室制取甲烷气体发生装置相同的是________.
①H2
②O2
③NH3
④NO
⑤Cl2
(2)现有如图所示的装置,可用它来收集CH4气体.收集时,配以不同的操作方法,会形成不同的收集方式.请简述CH4的三种收集方式.
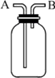
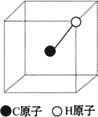
(3)已知CH4分子在空间呈四面体形状,1个C原子与4个H原子各共用一对电子形成4条共价键,C原子位于中心,4个H原子位于4个顶点.如图所示为一个立方体,已画出1个C原子(在立方体中心)、1个H原子(在立方体顶点)和1条共价键(实线表示),请画出另3个H原子的合适位置和3条共价键.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com