
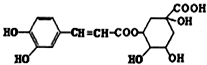
| A. | 分子中所有碳原子可能共面 | |
| B. | 一定条件下,1mol该物质最多与4molNaOH反应 | |
| C. | 水解产物都可以与FeCl3溶液发生显色反应 | |
| D. | 1mol该物质最多与6mol Br2反应 |
分析 由结构可知,分子中含酚-OH,碳碳双键、-COOC-、醇-OH、-COOH,结合酚、烯烃、酯、醇、羧酸的性质来解答.
解答 解:A.与-OH、-COOH相连的环中的C均为四面体结构,则不可能所有C原子共面,故A错误;
B.酚-OH、-COOC-、-COOH均与NaOH反应,则一定条件下,1mol该物质最多与4molNaOH反应,故B正确;
C.水解产物只有一种与FeCl3溶液发生显色反应,故C错误;
D.酚-OH的邻、对位与溴水发生取代反应,碳碳双键与溴水发生加成反应,则1mol该物质最多与4mol Br2反应,故D错误;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意常见有机物的性质,题目难度不大.


科目:高中化学 来源: 题型:解答题
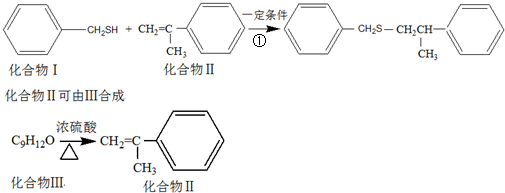
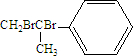 .
.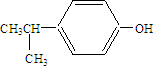 .
.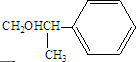 .化合物Ⅳ与新制Cu(OH)2反应的化学方程式
.化合物Ⅳ与新制Cu(OH)2反应的化学方程式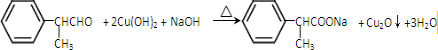 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
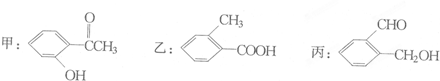
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
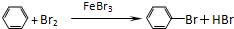 属于取代反应
属于取代反应 属于取代反应
属于取代反应 属于加聚 反应
属于加聚 反应查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验要求 | 实验方法 |
| 测定某工业废水的酸碱度 | |
| 检验自来水中残余氯分子 | |
| 检验CO2气体中含有的SO2 | |
| 除去FeCl2中的少量FeCl3 | |
| 除去NO中混有的少量NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | O2和O3互为同素异形体 | B. | O3是由3个氧原子构成的化合物 | ||
| C. | O2和O3相互转化属于化学变化 | D. | O3的摩尔质量为48g.mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
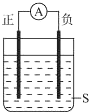
| A. | 正极Cu,负极Al,S为浓HNO3 | B. | 正极Ag,负极Al,S为NaOH | ||
| C. | 正极Ag,负极Cu,S为浓HCl | D. | 正极Zn,负极Cu,S为H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 铁氰化钾{K3[Fe(CN)6]}俗称赤血盐,常用于检验Fe3+,遇Fe2+生成深蓝色沉淀,离子反应方程式为:3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓.回答下列问题:
铁氰化钾{K3[Fe(CN)6]}俗称赤血盐,常用于检验Fe3+,遇Fe2+生成深蓝色沉淀,离子反应方程式为:3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com