


���� ��1���Ȼ�ˮ�ⷨ�����������������ᣬ���ԭ���غ������
��2���ٵ��ζ��ﵽ�յ�ʱNH4SCN������Fe3+��SCN-��Ӧ��Һ���ɫ��������ڲ���ɫ������ȷ���ζ��յ㣻
������AgSCN�������ܽ�ȱ�AgClС���ɼ�������������ҡ����ʹAgCl�������汻�л��︲�ǣ������ڵμ�NH4SCNʱ����AgCl����ת��ΪAgSCN���������˲�����NH4SCN��Һ����ƫ�ࣻ
��3�����ڳ���ǰ�ȼ�������Ư��ʹ��ˮ�е�H3PO3����ΪPO43-��������ʯ�Һ�����ȫת��Ϊ����ĸ��Σ��ﵽ�ϸߵĻ����ʣ�
�ڸ���ͼ1��2�����ij��������ʣ�
�۸���Ksp[Ca3��PO4��2]=[c��Ca2+��]3��c��PO43-�����㣮
��� �⣺��1���Ȼ�ˮ�ⷨ�������Ȼ��ס�������ˮ��Ӧ���������������ᣬ�仯ѧ����ʽΪ��PCl3+H2O+Cl2=POCl3+2HCl���ʴ�Ϊ��PCl3+H2O+Cl2=POCl3+2HCl��
��2������c mol•L-1NH4SCN��Һ�ζ�����Ag+���յ㣬���ζ��ﵽ�յ�ʱNH4SCN��������NH4Fe��SO4��2��ָʾ����Fe3+��SCN-��Ӧ��Һ����ɫ��������ڲ���ɫ������ȷ���ζ��յ㣻
�ʴ�Ϊ��b����Һ��Ϊ��ɫ�����Ұ�����ڲ���ɫ��
����֪��Ksp��AgCl��=3.2��10-10��Ksp��AgSCN��=2��10-12����AgSCN�������ܽ�ȱ�AgClС���ɼ�������������ҡ����ʹAgCl�������汻�л��︲�ǣ������ڵμ�NH4SCNʱ����AgCl����ת��ΪAgSCN���������˲�����NH4SCN��AgCl��Ӧ����AgSCN��������ζ�ʱ���ĵ�NH4SCN��Һ�����ƫ�࣬�������ӵ����ʵ���ƫ�����������ӷ�Ӧ�������ӵ����ʵ���ƫС�����Բ�õ������ӵ����ʵ���ƫС��
�ʴ�Ϊ����ֹ�ڵμ�NH4SCNʱ����AgCl����ת��ΪAgSCN������ƫС��
��3�����Ȼ�ˮ�ⷨ������������������ף���ҪΪH3PO4��H3PO3�ȣ���ˮ���ڷ�ˮ���ȼ�������Ư�ۣ�ʹ��ˮ�е�H3PO3����ΪPO43-��ʹ�������ʯ�Һ�����ȫת��Ϊ����ĸ��Σ��ﵽ�ϸߵĻ����ʣ�
�ʴ�Ϊ������ˮ�е�H3PO3����ΪPO43-��ʹ�������ʯ�Һ�ת��Ϊ����ĸ��Σ�
�ڸ���ͼ1��2��ȷ��pH=10����Ӧʱ��30 minʱ�ij��������ʽϸߣ������ó���ˮ����ʵĹ�������ΪpH=10����Ӧʱ��30 min��
�ʴ�Ϊ��bc��
����������ķ�ˮ��c��PO43-��=4��10-7 mol•L-1��Ksp[Ca3��PO4��2]=[c��Ca2+��]3��c��PO43-��=2��10-29��c��Ca2+��=$\root{3}{\frac{2��1{0}^{-29}}{��4��1{0}^{-7}��^{2}}}$=5��10-6mol•L-1��
�ʴ�Ϊ��5��10-6��
���� ���⿼�������ʵ��Ʊ�������ƣ���Ŀ�漰��ѧ����ʽ����д���ζ�ԭ����Ӧ�á�ͼ������Լ����ܵ���ʵ��ܶȻ�������Ӧ�õȣ���Ŀ�ۺ��Խ�ǿ���Ѷ��еȣ������ڿ���ѧ���ķ��������ͶԻ���֪ʶ���ۺ�Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ۢ� | C�� | �ڢ� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2Na+2H2O=2NaOH+H2�� | B�� | C12+H2O=HC1+HC1O | ||
| C�� | 2F2+2H2O=4HF+O2 | D�� | 2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2H2��+O2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
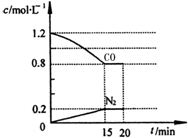 �½�����ġ�ǰ�ؿ�ѧ����־�������й�������ѧ�о�Ժ�о�Ա�����ġ�����β����Ⱦ����Σ����������ϵͳ�ز���������β���ŷŶԴ������������彡����ɵ�����Σ����Ŀǰ����β���Ŀ��з������������������ϰ�װ��ת������NO��CO�����Ϊ����β���ijɷ֣������������ڴ�ת�����з�����Ӧ��2CO��g��+2NO��g��?N2��g��+2CO2��g����H=-a kJ•mol-1��
�½�����ġ�ǰ�ؿ�ѧ����־�������й�������ѧ�о�Ժ�о�Ա�����ġ�����β����Ⱦ����Σ����������ϵͳ�ز���������β���ŷŶԴ������������彡����ɵ�����Σ����Ŀǰ����β���Ŀ��з������������������ϰ�װ��ת������NO��CO�����Ϊ����β���ijɷ֣������������ڴ�ת�����з�����Ӧ��2CO��g��+2NO��g��?N2��g��+2CO2��g����H=-a kJ•mol-1��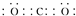 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 950mL 111.2g | B�� | 1000mL 117g | C�� | 1000mL 111.2g | D�� | 950mL 117g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | A2��g��+B2��g��?2AB��g����H��0 | B�� | 4NH3��g��+5O2��g��?4NO��g��+6H2O��g����H��0 | ||
| C�� | W��g��?Z��g����H��0 | D�� | 2SO3��g��?2SO2��g��+O2��g����H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ħ���������22.4 L/mol | |
| B�� | 1 mol H2������ֻ���ڱ���²�ԼΪ2 g | |
| C�� | ����£�18��H2O�����Ϊ22.4 L | |
| D�� | H2��O2�Ļ������1 mol�ڱ���µ����ԼΪ22.4 L |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com