
【题目】一定条件下,在体积不变的密闭容器中,能表示反应: X(g)+2Y(g) ![]() 2Z(g)一定达到化学平衡状态的是( )
2Z(g)一定达到化学平衡状态的是( )
①X、Y、Z的物质的量之比为1∶2∶2
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成n mol Z,同时生成2n mol Y
A.①②B.①④C.②③D.③④
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】用酸性氢氧燃料电池电解苦卤水![]() 含
含![]() 、
、![]() 、
、![]() 、
、![]() 的装置如图所示
的装置如图所示![]() 、b为石墨电极
、b为石墨电极![]() ,下列说法正确的是
,下列说法正确的是
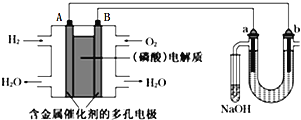
A.电池工作时,B极反应式为![]()
B.电解时,电子流动路径是:A极![]() 外电路
外电路![]() 极
极![]() 溶液
溶液![]() 极
极![]() 极
极
C.NaOH溶液充分吸收后所得溶液可制作漂白水
D.当电池中消耗![]() 标准状况
标准状况![]() 时,a极周围也会产生
时,a极周围也会产生![]() 标准状况
标准状况![]() 气体
气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是
A.常温下,10 mL pH=1的醋酸溶液中含有的氢离子数为0.001NA
B.合成氨反应中,1 mol N2与4 mol H2反应生成的NH3分子数为2NA
C.用碱性锌锰干电池作电源电解饱和食盐水,当消耗MnO2 8.7g时,可制得标况下氯气2.24L(不考虑氯气的溶解;电池工作时MnO2转化为MnOOH)
D.常温常压下,18.4 g NO2和N2O4的混合气体中含有的氮原子总数为0.8NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某可逆反应aA+bB![]() cC在某温度下的平衡常数为K(K≠1),反应热为ΔH。保持温度不变,将方程式的书写作如下改变,则ΔH和K数值的相应变化为( )
cC在某温度下的平衡常数为K(K≠1),反应热为ΔH。保持温度不变,将方程式的书写作如下改变,则ΔH和K数值的相应变化为( )
A.写成2aA+2bB![]() 2cC,ΔH值、K值均扩大了一倍
2cC,ΔH值、K值均扩大了一倍
B.写成2aA+2bB![]() 2cC,ΔH值扩大了一倍,K值保持不变
2cC,ΔH值扩大了一倍,K值保持不变
C.写成cC![]() aA+bB,ΔH值、K值变为原来的相反数
aA+bB,ΔH值、K值变为原来的相反数
D.写成cC![]() aA+bB,ΔH值变为原来的相反数,K值变为原来的倒数
aA+bB,ΔH值变为原来的相反数,K值变为原来的倒数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应COCl2(g)![]() CO(g)+Cl2(g) ΔH>0,达到平衡时,下列措施:
CO(g)+Cl2(g) ΔH>0,达到平衡时,下列措施:
①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
A.①②④B.①④⑥C.②③⑤D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,密闭容器中发生反应aX(g) ![]() bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍。则下列叙述正确的是
bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍。则下列叙述正确的是
A. 可逆反应的化学计量数:a>b+c
B. 达到新平衡时,物质X的转化率减小
C. 压缩容器的容积时,υ正增大,υ逆减小
D. 达到新平衡时,混合物中Z的质量分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1mol/LNaOH和0.1mol/LNH4Cl溶液等体积混合后,离子浓度大小正确的次序是( )
A.c(Na+)>c(Cl-)>c(OH-)>c(H+)
B.c(Na+)=c(Cl-)>c(OH-)>c(H+)
C.c(Na+)=c(Cl-)>c(H+)>c(OH-)
D.c(Cl-)>c(Na+)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.将纯水加热的过程中,Kw变大、pH变小
B.配制FeSO4溶液时,加入稀HNO3抑制Fe2+水解
C.FeCl3溶液蒸干、灼烧至恒重,最终得到FeCl3固体
D.向0.1mol/L氨水中加入少量水,溶液中![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】针对下图装置的说法中正确的是( )
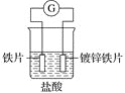
A. 溶液中pH明显下降
B. 铁片为正极,镀锌铁片为负极
C. 铁片的电极反应式:Fe-2e-=Fe2+
D. 电子由锌经溶液流向铁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com