
| 实验步骤与实验现象 | 实验结论 |
| Ⅰ.观察溶液:无色透明 | ①原溶液中一定不含的离子是Cu2+、MnO4-、Fe2+ |
| Ⅱ.取适量该溶液,加入过量的硝酸,有气体生成,并得到无色溶液 | ②原溶液中一定不含的离子是Mg2+、Ag+、Ba2+、Al3+、I-、SiO32-,一定含有的离子是CO32-、K+ |
| Ⅲ.在Ⅱ所得溶液中再加入过量的碳酸氢铵溶液,有气体生成,同时析出白色沉淀A | ③原溶液中还一定含有的离子是AlO2-,生成沉淀A的离子方程式为Al3++3HCO3-=Al(OH)3↓+3CO2↑ |
| Ⅳ.在Ⅲ所得溶液中再逐滴加入氢氧化钡溶液至过量,加热也有气体生成,同时析出白色沉淀B | ④白色沉淀B中一定含有BaCO3,可能含有BaSO4 |
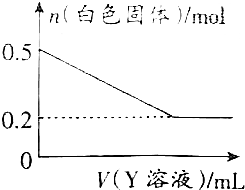
 (3)该化学兴趣小组的同学为了进一步确定B的成分,取一定量经洗涤后的B与Y溶液反应,白色固体的物质的量与Y溶液体积之间的关系如图所示.
(3)该化学兴趣小组的同学为了进一步确定B的成分,取一定量经洗涤后的B与Y溶液反应,白色固体的物质的量与Y溶液体积之间的关系如图所示.分析 I.观察溶液:无色透明,则一定不存在有色离子:Cu2+、MnO4-、Fe2+;
Ⅱ.取适量该溶液,加入过量的硝酸,有气体生成,该气体为二氧化碳,则溶液中一定存在CO32-,一定不存在与CO32-离子反应的Mg2+、Ag+、Ba2+、Al3+离子;得到无色溶液,则一定不存在I-、SiO32-,再根据溶液呈电中性判断原溶液中一定存在唯一阳离子K+;
Ⅲ.在Ⅱ所得溶液中再加入过量NH4HCO3溶液,有气体生成,同时析出白色沉淀A,说明溶液中一定存在铝离子,原溶液中一定存在AlO2-;
IV.在Ⅲ所得溶液中含有过量的碳酸氢铵,加入过量Ba(OH)2溶液至过量,加热会有氨气生成,白色沉淀可能为碳酸钡或碳酸钡和硫酸钡的混合物,
以此解答该题.
解答 解:(1)I.观察溶液:无色透明,则一定不存在有色离子:Cu2+、MnO4-、Fe2+;
Ⅱ.取适量该溶液,加入过量的硝酸,有气体生成,该气体为二氧化碳,则溶液中一定存在CO32-,一定不存在与CO32-离子反应的Mg2+、Ag+、Ba2+、Al3+离子;得到无色溶液,则一定不存在I-、SiO32-,再根据溶液呈电中性判断原溶液中一定存在唯一阳离子K+;
Ⅲ.在Ⅱ所得溶液中再加入过量NH4HCO3溶液,有气体生成,同时析出白色沉淀A,说明溶液中一定存在铝离子,原溶液中一定存在AlO2-,反应的离子方程式为Al3++3HCO3-=Al(OH)3↓+3CO2↑,
IV.在Ⅲ所得溶液中含有过量的碳酸氢铵,加入过量Ba(OH)2溶液至过量,加热会有氨气生成,白色沉淀可能为碳酸钡或碳酸钡和硫酸钡的混合物,
故答案为:
| 实验步骤和实验现象 | 实验结论 |
| Ⅰ.观察溶液:无色 | ①Cu2+、MnO4-、Fe2+ |
| Ⅱ.取适量该溶液,加入过量的硝酸,有气体生成,并得到无色溶液 | ②Mg2+、Ag+、Ba2+、Al3+、I-、SiO32-;CO32-、K+ |
| Ⅲ.在Ⅱ所得的溶液中再加入过量的碳酸氢铵溶液,有气体生成,同时析出白色沉淀A | ③AlO2-;Al3++3HCO3-=Al(OH)3↓+3CO2↑ |
| Ⅳ.在Ⅲ所得溶液中再逐滴加入氢氧化钡溶液至过量,加热也有气体生成,同时析出白色沉淀B | ④BaCO3;BaSO4 |
点评 本题考查无机物的推断,为高考常见题型,侧重于学生的分析能力的考查,题目涉及离子共存、常见离子的检验,题目难度中等,试题的题量较大,注意掌握常见离子的性质及检验方法,明确离子反应发生的条件及离子共存的条件.


科目:高中化学 来源: 题型:选择题
| A. | 锗是一种金属性很强的元素 | B. | 锗酸(H4GeO4)是难溶于水的强酸 | ||
| C. | 锗化氢(GeH4)稳定性很强 | D. | 锗的单质具有半导体的性能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol Fe在0.1mol Cl2中充分燃烧,转移电子数为0.3NA | |
| B. | 用MnO2与浓盐酸制取Cl2时,每生成1 mol Cl2则转移电子数为NA | |
| C. | 1L 0.1mol•L-1(NH4)2SO4溶液中含有NH4+的数目为0.2 NA | |
| D. | 23g钠在足量氧气中充分燃烧,转移电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤和实验现象 | 实验结论 |
| Ⅰ.观察溶液:无色 | ①原液中一定不含的离子是: Cu2+、MnO4-、Fe2+ |
| Ⅱ.取适量该溶液,加入过量的硝酸,有气体生成,并得到无色溶液 | ②原液中一定不含的离子是: Mg2+、Ag+、Ba2+、Al3+、I-、SiO32- 一定含的离子是: CO32-、K+ |
| Ⅲ.在Ⅱ所得的溶液中再加入过量的碳酸氢铵溶液,有气体生成,同时析出白色沉淀A | ③原液中还一定含有的离子是: AlO2-生成沉淀A的离子方程式为: AlO2-+HCO3-+H2O=CO32-+Al(OH)3↓ |
| Ⅳ.在Ⅲ所得溶液中再逐滴加入氢氧化钡溶液至过量,加热也有气体生成,同时析出白色沉淀B | ④白色沉淀B中一定含有: BaCO3可能含有: BaSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 铝热剂的反应原理是利用铝的强还原剂 | |
| B. | 铝热剂的反应常用于冶炼难熔金属 | |
| C. | 铝热剂发生的铝热反应需要用镁带和氯酸钾引燃,所以是一个吸热反应 | |
| D. | 铝和所有金属物都可以组成铝热剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔质量就等于物质的式量 | |
| B. | 摩尔质量就是物质式量的6.02×1023倍 | |
| C. | HNO3的摩尔质量是63g | |
| D. | 硫酸和磷酸的摩尔质量相等,都是98g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去NaHCO3溶液中少量的Na2CO3:通入过量的CO2 | |
| B. | 胶体是一种能产生丁达尔效应的分散系 | |
| C. | 纯碱不属于碱,干冰属于酸性氧化物 | |
| D. | Na2O和Na2O2都能与水反应生成对应的碱,它们都是碱性氧化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com