
【题目】反应A(g)+B(g) ![]() C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
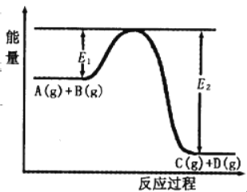
(1)该反应是______反应(填“吸热”“放热”);
(2)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1______,E2______(填“增大”“减小”、“不变”)。
(3)反应体系中加入催化剂对反应热是否有影响?______,(填“是”或“否”)原因是_______________。
(4)该反应的反应热△H=__________kJ/mol。(用E1和E2表示)
科目:高中化学 来源: 题型:
【题目】已知A是一种重要的基本化工原料,能使溴的四氯化碳溶液褪色,其产量常用于衡量一个国家石油化工发展水平的标志,也是一种植物生长调节剂。下列是有机物A~G之间的转化关系:

请回答下列问题:
(1)B的官能团的名称是 ,G是一种高分子化合物,其链节是 。
(2)由A生成F的反应类型是 反应,B生成C的化学方程式是 。
(3)B和D反应生成E的化学方程式是 ,该反应类型是反应 。
(4)工业上用30吨D与46吨B反应,如果实际产率是理论产率的67%,则实际可得到的E的质量是 (保留四位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机高分子化合物甲是一种常用的光敏高分子材料,其结构简式为:
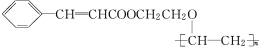
按下图流程可以合成甲,其中试剂Ⅰ可由相对分子质量为26的烃与水加成制得。
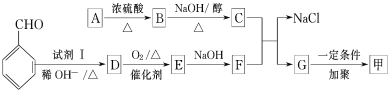
已知:
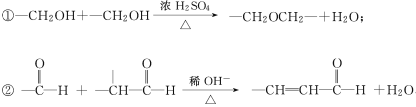
回答下列问题:
(1)质谱图显示A的相对分子质量是80.5。A分子中氧元素的质量分数为19.88%,碳元素的质量分数为29.81%,其余为氢元素和氯元素。A的核磁共振氢谱上有三个吸收峰,峰面积的比例为2∶2∶1。A的结构简式为 。
(2)试剂Ⅰ的名称是________________;B→C的反应类型是________________。
(3)写出下列反应的化学方程式:
①A→B:________________________;
②D→E:________________________;
③C与F的反应:________________________。
(4)E的一种同分异构体,水解产物有两种,一种能使溴水褪色,另一种在滴加饱和溴水后,有白色沉淀生成,该物质的结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于NH4+、NH3、NH2-三种微粒的说法不正确的是
A.三种微粒所含有的电子数相等
B.三种微粒中氮原子的杂化方式相同
C.三种微粒的空间构型相同
D.键角大小关系:NH4+>NH3>NH2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.以下是元素周期表的一部分,根据图示回答下列问题:
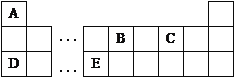
(1)将16.25gFeCl3投入足量A2C2溶液中,产生大量气泡,反应完全后,FeCl3的质量为__________g。
(2)1.3gB2A2气体完全燃烧,恢复至室温,放出65kJ热量,写出代表B2A2燃烧热的热化学反应方程式_____________________________________________________________。
(3)D的最高价氧化物的水化物与E的最高价氧化物的水化物反应的离子方程式为:
_____________________________________________________________。
II.X、Y、Z、W四种元素是周期表前四周期元素,X原子的核外有16种不同运动状态的电子,Y的原子序数比X大1,Z原子的外围电子排布式为3d64s2,W的价层电子排布式为ndn+5(n+1)sn-1。
(4)X在元素周期表中的位置___________________________;W元素的名称为_________。
(5)XY2分子中各原子均满足8电子稳定结构,画出XY2的电子式____________。
(6)电负性X_______Y;Z的原子结构示意图为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究氮及其化合物的转化在实际工业生产、生活中具有重要的意义。
(1)已知![]()
![]()
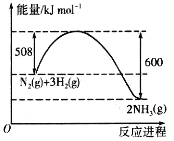
![]() 的能量变化如图所示,在一定温度下,向2L的恒容密闭容器中投入2.2 molN2和2.6 mol H2,经10 min达到平衡,测得放出的热量为18.4 kJ,则
的能量变化如图所示,在一定温度下,向2L的恒容密闭容器中投入2.2 molN2和2.6 mol H2,经10 min达到平衡,测得放出的热量为18.4 kJ,则![]() ______。该温度下,反应的平衡常数K=________(mol·L-1)-2。平衡后,再向体系中投入1.1 mol N2和1.3 mol H2,重新达到平衡后N2的体积分数________(填“增大”“减小”或“不变”)。
______。该温度下,反应的平衡常数K=________(mol·L-1)-2。平衡后,再向体系中投入1.1 mol N2和1.3 mol H2,重新达到平衡后N2的体积分数________(填“增大”“减小”或“不变”)。
(2)利用炽热的活性炭可以处理NO2,反应原理为![]()
![]()
![]() 。
。
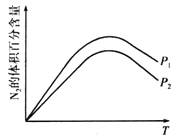
①探究温度、压强对该反应的影响如图所示,则该反应的![]() ___________0(填“>”“<”或“=”),P1_____________P2(填“>”“<”或“=”)。
___________0(填“>”“<”或“=”),P1_____________P2(填“>”“<”或“=”)。
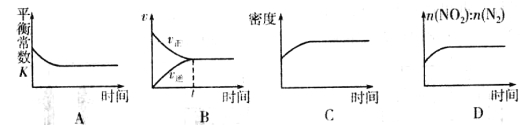
②一定温度下,将一定量的活性炭和NO2加入一恒容密闭容器中,下列示意图正确且能说明反应达到平衡状态的是____________(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
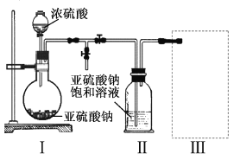
实验一焦亚硫酸钠的制取
采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置II中有Na2S2O5晶体析出,发生的反应为:
Na2SO3+SO2=Na2S2O5
(1)装置I中产生气体的化学方程式为 。
(2)要从装置II中获得已析出的晶体,可采取的分离方法是 。
(3)装置III用于处理尾气,可选用的最合理装置(夹持仪器已略去)为 。(填序号)。
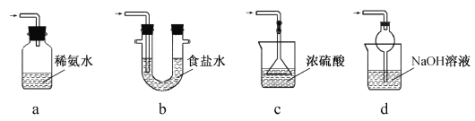
实验二焦亚硫酸钠的性质
Na2S2O5溶于水即生成NaHSO3。
(4)检验Na2S2O5晶体在空气中已被氧化的实验方案是 。
实验三葡萄酒中抗氧化剂残留量的测定
(5)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:馏分中的二氧化硫在滴入碘水时发生的反应为
SO2+I2+2H2O=H2SO4+2HI)在测定时消耗了0.01mol·L-1的I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为 g·L-1。在上述实验过程中,若有部分HI被空气氧化,则测得结果 (填“偏高”“偏低”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com