
����п���Ʊ�ӫ��۵�ԭ��֮һ����ҵ����п����Ҫ�ɷ���ZnO��������Fe2O3��CuO��SiO2�����ʣ��Ʊ�ZnSO4?7H2O���������¡�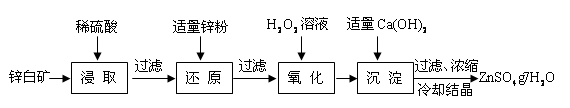
��֪�������£���Һ�е�Fe3+��Zn2+��Fe2+������������ʽ��ȫ������pH�ֱ�Ϊ��3.7��6.5��9.7��
��1����ȡ��������߽���Ч�ʿɲ��õĴ�ʩ���������δ�һ������
ZnO�����ᷴӦ�Ļ�ѧ����ʽΪ������
��2����������п�۵�����Ϊ����ʹ��Һ�е�Fe3+ת��ΪFe2+����������
��3������������H2O2������Ӧ�����ӷ���ʽΪ������
��4����������Ca(OH)2������ҺpH���ٽ�Fe3+ˮ�⣬Fe3+ˮ�ⷴӦ��ƽ�ⳣ������ʽ
K��������Ca(OH)2���ܹ�����ԭ����������
��12�֣�
��1������ʯ�������߽�ȡ�¶Ȼ��ʵ��������Ũ�ȵȣ�2�֣�
ZnO+H2SO4=ZnSO4+H2O��2�֣�
��2����ȥCu2+��2�֣�
��3��H2O2+2Fe2++2H+=2Fe3++2H2O��2�֣�
��4��c3(H+)/c(Fe3+) ��2�֣� ��ֹ����Zn(OH)2��2�֣�
���������������1��������������ͬ�����������Ҫ�ɷݷ�Ӧ���ӻ�ѧ��Ӧ���ʺͻ�ѧƽ���Ӱ��������������ͨ�������¶��������п���ܽ�ȣ���ͨ������ʹ��Ӧ���ֽӴ���Ӧ����ͨ�����˺�������ν�ȡ�����ת���ʣ��ʴ�Ϊ���ʵ���߷�Ӧ�¶ȡ����ӽ���ʱ�䣨�����������𰸣���ZnO�����ᷴӦ�Ļ�ѧ����ʽΪZnO+H2SO4=ZnSO4+H2O���ʴ�Ϊ�� ZnO+H2SO4=ZnSO4+H2O���Ƽ���п�ۣ��������·�Ӧ��Zn��2H��=Zn2����H2����Zn��2Fe3��=2Fe2����Zn2�� ,Fe��Cu2�� =Cu��Zn2�� ,Zn������Fe2����Zn=Fe��Zn2�� ��������Ŀ�м���������п�ۣ��ڳ�ȥCu2�� ���𰸣���ȥCu2+����H2O2��Fe2�� ������Fe3�� ������pH�ϵ͵������£�����ˮ���ȥFe3�� ���𰸣�H2O2+2Fe2++2H+=2Fe3++2H2O���ȸ���ˮ�ⷽ��ʽFe3����3H2O Fe(OH)3��3H�� ,д��ƽ�ⳣ��K= c3(H+)/c(Fe3+) ��Ca(OH)2���ܹ�����ԭ���ǣ�Fe3�� ��pHΪ1.1�D3.2ʱ������pH��5.9�D8.9ʱZn2�� �������𰸣�c3(H+)/c(Fe3+)����ֹ����Zn(OH)2��
Fe(OH)3��3H�� ,д��ƽ�ⳣ��K= c3(H+)/c(Fe3+) ��Ca(OH)2���ܹ�����ԭ���ǣ�Fe3�� ��pHΪ1.1�D3.2ʱ������pH��5.9�D8.9ʱZn2�� �������𰸣�c3(H+)/c(Fe3+)����ֹ����Zn(OH)2��
���㣺Ԫ�ػ�����֪ʶ���������ա���ѧƽ��ԭ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
����A�����ᣬB�����ᣬ C�����������ᣬ�������������ź͡�������������������ա�
��1����ͬ�����ͬpH���������У��ֱ����������NaHCO3��ĩ������ͬ�����²���CO2������ɴ�С��˳���� ��
��2����ͬ�����ͬ���ʵ���Ũ�ȵ��������У��ֱ����������NaHCO3��ĩ������ͬ�����²���CO2������ɴ�С��˳���� ��
��3�����ʵ���Ũ�Ⱦ�Ϊ0��1mol/L����������Һ��pH�ɴ�С��˳���� �����ȡ�������0��1mol/L����������Һ����0��1mol/L��NaOH�кͣ���ǡ����ȫ��Ӧʱ������NaOH��Һ������ɴ�С��˳���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���������ʢ�Cu����Һ̬SO2����CH3COOH����NaHCO3����Ba(OH)2��Һ��������NaCl����ϡ��ˮ����BaSO4����H2O
��1������ǿ����ʵ��� ������ţ� ����������ʵ��� ������ţ�
��2�������£�0.1 mol��L-1NaHCO3��Һ��pH����8������Һ��Na����HCO3�D��CO32�D��OH�D��������Ũ���ɴ�С��˳��Ϊ�� ��NaHCO3ˮ������ӷ���ʽ ��
��3��Ba(OH)2��һ��ǿ����ʣ�����25�桢pH��13��Ba(OH)2��Һ��
�ٸ�Ba(OH)2��Һ�����ʵ���Ũ��Ϊ___________________��
����ijŨ��������Һ������ȣ�������֮�ȣ�1 ��9��Ϻ�������ҺpH��11����������Һ��������ڻ��ǰ����Һ������ͣ�����������Һ��pH��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
����һ�仰������������ֵ��ǰ��ΪM������ΪN��M��N�Ĺ�ϵ��A��B��C��D ��ѡ��
A��M>N B��M<N C�� M="N" D�� ���Ƚ�
��1����ͬ�¶��£�1L 1mol/L ��NH4Cl��Һ��2 L 0.5mol��L��1NH4Cl��Һ������Һ��NH4+�ĸ����� ��
��2����ͬ�¶��£�pHֵΪ12���ռ���Һ��CH3COONa��Һ������Һ��ˮ�ĵ���̶ȣ� ��
��3�����������ݵ�Ũ�ȵĴ�����Һ�����ڶ��������¶ȣ�����Һ��c(HCO3��)�� ��
��4����pHֵΪ2�Ĵ�������ᶼϡ����ͬ��������ϡ��Һ��pHֵ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�������������ѧ��ѧ�г������ᣬ��һ�������£�CH3COOH��Һ�д��ڵ���ƽ�⣺CH3COOH CH3COO-+H+ ��H��0��
CH3COO-+H+ ��H��0��
��1�������£��� pH =5��ϡ������Һ�У�c(CH3COO-)��____________(��ʽ�����ػ���)�����з����У�����ʹ0��10 mol��L-1 CH3COOH�ĵ���̶��������______?
a����������0��10 mol��L-1��ϡ���� b������CH3COOH��Һ
c����ˮϡ����0��010 mol��L-1 d����������������
e�����������Ȼ��ƹ��� f����������0��10 mol��L-1��NaOH��Һ
��2������������пͶ��������pH������3�Ĵ����������Һ�У�������ַ�Ӧ����ֻ��һ����Һ����п��ʣ�࣬�����������������V(����)_________V(����)����Ӧ���������Ϊ��v(����)_________v(����)��(��д������������������)
��3��ijͬѧ��0��1000mol/LNaOH��Һ�ֱ�ζ�20��00mL 0��1000mol/LHCl��20��00mL0��1000mol/L CH3COOH���õ���ͼ��ʾ�����ζ����ߣ�������й����⣺
��NaOH��Һ�ζ�CH3COOH��Һ�������� ���ͼ1����ͼ2������
��a�� mL��
��4�������£���0��1 mol/L�����0��1 mol/L��������Һ��ϣ�������ҺΪ���ԣ�������Һ�и����ӵ�Ũ�Ȱ��ɴ�С����Ϊ_______________________________��
��5����֪��90��ʱ��ˮ�����ӻ�����ΪKw = 3��80��10-13���ڴ��¶��£���pH=3�������
pH = 11������������Һ�������ϣ�������Һ�е�c(H+)=____________(������λ��Ч����)mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�ظ����ι㷺������������Ƥ�������ȡ��Ը���ʯ����Ҫ�ɷ���Cr2O3����FeO��Al2O3�� SiO2������)Ϊԭ����ȡ�ظ����Ƶ��������£�
��ش��������⣺
��1��д��Cr2O3�ڸ��±���ʱ��Ӧ�Ļ�ѧ����ʽ______________________
��2��д�������ữʹNa-2CrO4ת��ΪNa2Cr2O7�����ӷ���ʽ ______________��
��3��ij��������ʯī�缫���Na2CrO4��Һ��ʵ ���� Na2CrO4�� Na2Cr2O7��ת������ԭ����ͼ��ʾ��
�������ӽ���Ĥ��һ�ֲ����Ǿ۱�ϩ����( )���۱�ϩ���Ƶ���Ľṹ��ʽ��________��
)���۱�ϩ���Ƶ���Ľṹ��ʽ��________��
��д�������ĵ缫��Ӧʽ__________
��4�� Na2Cr2O7�����ڲⶨ��ˮ�Ļ�ѧ����������COD��ָÿ��ˮ���л�ԭ�����ʱ����� ����ҪO2��������������ijˮ��100��00 mL���ữ�����C1 mol/L��Na2Cr2O7��Һ V1 mL��ʹˮ�еĻ�ԭ��������ȫ��������Cr2O72-��ԭΪCr3+��������C2mol/L��FeSO4��Һ�ζ�ʣ ���Cr2O72-���������FeSO4��ҺV2 mL��
�ٸ�ˮ����CODΪ______________mg/L��
�ڼ���������Ӧ��������Һ��Fe3+��Cr3+�����ʵ���Ũ�Ⱦ�Ϊ0��1 mol/L��ҪʹFe3 +�� ����ȫ��Cr3+��δ��ʼ���������������ҺpH�ķ�Χ�� _______��
(�����õ������ݣ�KSPFe(OH)3=4��0��10-38, KSPCr(OH)3=6��0��10-31��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�������ƣ�NaClO2��������ˮ��������ɰ�ǡ���֬��Ư����ɱ�����������ù������ⷨ�����������ƵĹ�������ͼ��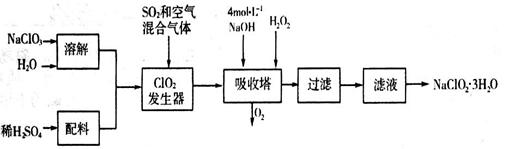
��֪��NaClO2���ܽ�����¶����߶������ʵ������¿ɽᾧ����NaClO2��3H2O��
��1���������ڷ�����Ӧ�Ļ�ѧ����ʽΪ_____________________����ƽ��ѧ����ʽ�����ù��������е�NaClO3��ClO2��NaClO2����ǿ�����������Ƕ��ܺ�Ũ���ᷴӦ��ȡCl2�����ö������Ⱥ�Ũ������ȡCl2��������5 mol Cl2ʱ��ͨ����ԭ��Ӧ�Ƶ�����������Ϊ________�ˡ�
��2������Һ�еõ���NaClO2��3H2O����IJ���������__________����д��ţ���
a.���� b.���� c.���� d.��ȴ�ᾧ
��3��ӡȾ��ҵ�����������ƣ�NaClO2��Ư��֯�Ư��֯��ʱ���������õ���HClO2���±���25��ʱHClO2�����ֳ�������ĵ���ƽ�ⳣ����
�ٳ����£����ʵ���Ũ����ȵ�NaClO2��NaF��NaCN��Na2S������Һ��pH�ɴ�С��˳��Ϊ____________�������ȣ����ʵ���Ũ����ͬ��NaF��NaCN����Һ�������������������Ĵ�С��ϵΪ��______________���ǰ�ߴ���ȡ����ߴ���
��Na2S�dz��õij�������ij��ҵ��ˮ�к��е�Ũ�ȵ�Cu2+��Fe2+��Pb2+���ӣ��μ�Na2S��Һ�����������ij�����_______�������һ�����ӳ�����ȫʱ��������Ũ��Ϊ10-5mol��L-1����ʱ��S2-��Ũ��Ϊ____��
��֪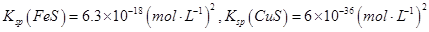
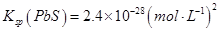
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ʴ���
�ơ�þ������ͭ���仯�����ڿ��к������������й㷺��Ӧ�á�
��1��Mg��H2O2��ؿ������������˼�ʻ��DZ�������õ���Ժ�ˮΪ�������Һ���ṹ��ͼ��ʾ����ع���ʱ�������ĵ缫��Ӧʽ �������£��øõ�ص��200mL�ı�������ͭ��Һ(�缫Ϊ���Ե缫)����Ӧʱ��Һ��ˮ�ĵ���ƽ�� �ƶ�(��������ҡ�����)��������24mg����Mg��������Һ��pH= (��������Һ������仯)��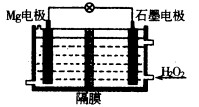
��2�����õ�ⷨ������Ʒ�϶�ͭ���Է�ֹ������ʴ������˵����ȷ���� ��
a�����ʱ��ͭ��ʯī��������������������ͭ�����������Һ
b����ƹ����У��¶����ߣ���ⷴӦ���ʼӿ�
c����ƹ����У�����ȫ��ת��Ϊ��ѧ��
d����ƹ����У�ͭ�����������ƶ���������ԭ��Ӧ
��3��NaHS����Ϊ��������ȥ��Һ�е�Cu2+�������£�NaHS��Һ�Լ��ԣ�ԭ���� (�����ӷ���ʽ�ͱ�Ҫ������˵��)������Cu2+�ķ�ˮ�м�������NaHS���壬��ˮ��Һ��pH (�������С�����䡱)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
ijѧ����0.200 0 mol��L��1�ı�NaOH��Һ�ζ�δ֪Ũ�ȵ����ᣬ�����Ϊ���¼�����
��������ˮϴ�Ӽ�ʽ�ζ��ܣ�������ע��NaOH��Һ����0���̶�������
�ڹ̶��õζ��ܲ�ʹ�ζ��ܼ������Һ��
�۵���Һ������0����0���̶�������ijһ�̶ȣ������¶���
����ȡ20.00 mL����Һע��ྻ����ƿ�У�������3�η�̪��Һ
���ñ�Һ�ζ����յ㣬���µζ���Һ�����
��ش�
(1)���ϲ����д������(����) ���ô�������ᵼ�²ⶨ���(�ƫ����ƫС������Ӱ�족) ��
(2)�жϵζ��յ�������ǣ���ƿ����Һ�� ɫ��Ϊ ɫ���Ұ�����ڲ���ɫ��
(3)��ͼ��ij�εζ�ʱ�ĵζ����е�Һ�棬�����Ϊ mL��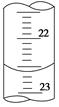
(4)�����������ݣ���������������Һ��Ũ��Ϊ mol/L
| �ζ����� | ����Һ���(mL) | ��NaOH��Һ������¼(mL) | |
| �ζ�ǰ���� | �ζ������ | ||
| ��һ�� | 20.00 | 0.40 | 20.40 |
| �ڶ��� | 20.00 | 4.00 | 24.00 |
| ������ | 20.00 | 2.00 | 24.10 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com