
分析 (1)平衡常数只受温度影响,将化学平衡常数K增大,应使平衡向正反应移动,该反应正反应是放热反应,故应降低温度,化学反应速率降低,据此解答;
(2)提高反应中Cl2的平衡转化率,改变条件使平衡向正反应移动,根据平衡移动原理结合选项分析解答,注意不能只增大氯气的用量;
(3)增大氯气的浓度,平衡向正反应移动,反应为可逆反应,反应物不能完全反应,平衡时37Cl存在37Cl2和SO237Cl2 中;
(4)达到平衡状态时,正逆反应速率相等,各物质的浓度不变,百分含量不变,以及由此衍生其它一些物理量不变,据此结合选项判断.
解答 解:(1)平衡常数只受温度影响,将化学平衡常数K增减小,该反应正反应是放热反应,故应升高温度,化学反应速率加快,化学反应速率v正增大,故选a,故答案为:a;
(2)提高反应中Cl2的平衡转化率,改变条件使平衡向正反应移动,不能只增大氯气的用量,
a.缩小容器体积,压强增大,平衡向正反应移动,Cl2的转化率增大,故a正确;
b.使用催化剂,缩短到达平衡的时间,不影响平衡移动,Cl2的转化率不变,故b错误;
c.增加SO2浓度,平衡向正反应移动,Cl2的转化率增大,故c正确;
d.该反应正反应是放热反应,升高温度,平衡向逆反应移动,Cl2的转化率降低,故d错误;
故答案为:ac;
(3)增大氯气的浓度,平衡向正反应移动,反应为可逆反应,氯气不能完全反应,故平衡时37Cl存在37Cl2和SO237Cl2 中,
故答案为:c;
(4)a.υ(Cl2)=υ(SO2),没有指明正、逆速率,无法判断,故a错误;
b.随反应进行,气体的物质的量减小,压强减小,容器中气体压强不随时间而变化,说明达到平衡,故b正确;
c.平衡时氯气与二氧化硫的浓度与起始浓度有关,起始浓度不同,平衡时二者浓度不同,若二者起始浓度相同,用于二者按1:1反应,故任意时刻二者的浓度都相同,故c(Cl2):c(SO2)=1:1不能说明达到平衡,故c错误;
d.容器中气体颜色不随时间两变化,说明氯气的浓度不再变化,说明达到平衡,故d正确;
故答案为:bd.
点评 本题考查化学平衡常数、影响反应速率的因素、化学平衡状态的判断、化学平衡影响因素等,难度中等,化学平衡状态的判断可用未平衡时是变量如果不变,说明达平衡状态.


科目:高中化学 来源: 题型:填空题
 ,它是汽油燃烧品质抗震性能的参照物,用系统命名法对它命名2,2,4-三甲基戊烷,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:
,它是汽油燃烧品质抗震性能的参照物,用系统命名法对它命名2,2,4-三甲基戊烷,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为: ;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简式为CH2=C(CH3)CH2C(CH3)3或(CH3)2C=CH(CH3)3.
;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简式为CH2=C(CH3)CH2C(CH3)3或(CH3)2C=CH(CH3)3.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
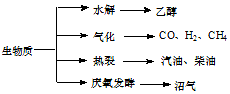 生物质资源是一种污染小的可再生能源,生物质的主要转化途径及主要产物如图.
生物质资源是一种污染小的可再生能源,生物质的主要转化途径及主要产物如图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高纯度的硅广泛用于制作光导纤维,其遇强碱会“断路” | |
| B. | 焰火的五彩缤纷是某些金属元素物理性质的展现 | |
| C. | “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化 | |
| D. | 食盐、次氯酸钠溶液均可以将某些病毒氧化而达到消毒的目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应①属于非氧化还原反应 | |
| B. | 反应②属于非氧化迩原友应 | |
| C. | 反应④中TiO2是氧化剂 | |
| D. | 反应⑤表现了金属镁还原性比进士钛强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,它可能具有的性质是( )
,它可能具有的性质是( )| A. | 不易溶于水,易溶于苯等有机溶剂 | B. | 是芳香烃,也是苯的同系物 | ||
| C. | 能发生聚合反应,其产物可表示为 | D. | 分子中所有碳原子一定在同一平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下饱和CO2溶液的pH约为5.6.向某未知浓度的Na2CO3溶液中滴入已知浓度的盐酸时,用 pH传感器测得混合溶液的pH变化曲线如图所示,下列说法正确的是( )
常温下饱和CO2溶液的pH约为5.6.向某未知浓度的Na2CO3溶液中滴入已知浓度的盐酸时,用 pH传感器测得混合溶液的pH变化曲线如图所示,下列说法正确的是( )| A. | 该Na2CO3溶液的浓度为0.001mol/L | |
| B. | 在pH=7时,c(Na+)>c(Cl-) | |
| C. | 在pH=6时,c(Na+)>c(CO32-)>c(HCO3-) | |
| D. | c→d发生的主要离子反应为:CO32-+H+=HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com