
·ÖĪö Č¼ĮĻµē³ŲŹĒ»ÆѧÄÜÖ±½Ó×Ŗ»ÆĪŖµēÄܵÄ×°ÖĆ£¬²»ŠčŅŖ¾¹żČČÄÜÕāŅ»ÖŠ¼äŠĪŹ½£»
£Ø1£©ĒāŃõČ¼ĮĻµē³ŲÖŠĒāĘųŌŚøŗ¼«Ź§µē×Ó·¢ÉśŃõ»Æ·“Ó¦£¬ŌŚ¼īŠŌ»·¾³ÖŠ½įŗĻĒāŃõøłĄė×ÓÉś³ÉĖ®£¬ŃõĘųŌŚÕż¼«µĆµē×Ó·¢Éś»¹Ō·“Ӧɜ³ÉĒāŃõøłĄė×Ó£¬¾Ż“Ė·ÖĪö£»
£Ø2£©1LĖ®ŌŚ³£ĪĀĻĀµÄÖŹĮæĪŖ1000g£¬ĒāŃõČ¼ĮĻµē³ŲµÄ×Ü·“Ó¦ĪŖ£ŗ2H2+O2=2H2O£¬Éś³É36gĖ®»į°éĖę×Å4molµē×Ó×ŖŅĘ£¬¾Ż“Ė¼ĘĖć£®
½ā“š ½ā£ŗČ¼ĮĻµē³ŲŹĒ»ÆѧÄÜÖ±½Ó×Ŗ»ÆĪŖµēÄܵÄ×°ÖĆ£¬²»ŠčŅŖ¾¹żČČÄÜÕāŅ»ÖŠ¼äŠĪŹ½£¬¹Ź“š°øĪŖ£ŗ»Æѧ£»µē£»ČČ£»
£Ø1£©A”¢ĒāŃõČ¼ĮĻµē³ŲÖŠĒāĘųŗĶŃõĘų²»ŹĒÖ±½Ó·“Ó¦£¬ŹĒ»ÆѧÄÜÖ±½Ó×Ŗ»ÆĪŖµēÄܵÄ×°ÖĆ£¬²»ŠčŅŖ¾¹żČČÄÜÕāŅ»ÖŠ¼äŠĪŹ½£¬¹ŹA“ķĪó£»
B”¢ĒāŃõČ¼ĮĻµē³ŲÖŠĒāĘųŌŚøŗ¼«·“Ó¦£¬ŃõĘųŌŚÕż¼«·“Ó¦£¬¹ŹB“ķĪó£»
C”¢ĒāŃõČ¼ĮĻµē³Ų·“Ӧɜ³ÉĖ®£¬Ź¹KOHČÜŅŗÅØ¶Č¼õŠ”£¬¼īŠŌ¼õČõ£¬¹ŹC“ķĪó£»
D”¢ĒāŃõČ¼ĮĻµē³ŲÖŠĒāĘųŌŚøŗ¼«Ź§µē×Ó·¢ÉśŃõ»Æ·“Ó¦£¬ŃõĘųŌŚÕż¼«µĆµē×Ó·¢Éś»¹Ō·“Ó¦£¬¹ŹDÕżČ·£»
¹Ź“š°øĪŖ£ŗD£»
£Ø2£©ĒāŃõČ¼ĮĻµē³ŲµÄ×Ü·“Ó¦ĪŖ£ŗ2H2+O2=2H2O£¬Éś³É36gĖ®»į°éĖę×Å4molµē×Ó×ŖŅĘ£¬½ńÓūµĆ³£ĪĀĻĀĖ®1L¼“1000g£¬
×ŖŅʵē×ÓŹĒ$\frac{1000”Į4}{36}$mol=1.1”Į102mol£®
¹Ź“š°øĪŖ£ŗC£®
µćĘĄ ±¾Ģāæ¼²éŃ§ÉśČ¼ĮĻµē³ŲµÄ¹¤×÷ŌĄķŅŌ¼°µē³Ų·“Ó¦ŗĶµē×Ó×ŖŅĘµÄ¼ĘĖćÖŖŹ¶£¬×¢ŅāÖŖŹ¶µÄĒØŅĘŗĶÓ¦ÓĆŹĒ¹Ų¼ü£¬ÄŃ¶Č²»“ó£®


 ABCæ¼ĶõČ«ÓžķĻµĮŠ“š°ø
ABCæ¼ĶõČ«ÓžķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ŅŃÖŖA”¢B”¢C”¢D¾łĪŖĒ°ĖÄÖÜĘŚŌŖĖŲĒŅŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ŌŖĖŲAµÄ»łĢ¬Ō×Ó2p¹ģµĄÓŠ3øöĪ“³É¶Ōµē×Ó£¬ŌŖĖŲBµÄŌ×Ó×īĶā²ćµē×ÓŹżŹĒĘäÄŚ²ćµē×ÓŹżµÄ3±¶£¬ŌŖĖŲCµÄŅ»ÖÖ³£¼ūµ„ÖŹĪŖµ»ĘÉ«·ŪÄ©£¬DµÄÄŚ²ć¹ģµĄČ«²æÅÅĀśµē×Ó£¬ĒŅ×īĶā²ćµē×ÓŹżĪŖl£®
ŅŃÖŖA”¢B”¢C”¢D¾łĪŖĒ°ĖÄÖÜĘŚŌŖĖŲĒŅŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ŌŖĖŲAµÄ»łĢ¬Ō×Ó2p¹ģµĄÓŠ3øöĪ“³É¶Ōµē×Ó£¬ŌŖĖŲBµÄŌ×Ó×īĶā²ćµē×ÓŹżŹĒĘäÄŚ²ćµē×ÓŹżµÄ3±¶£¬ŌŖĖŲCµÄŅ»ÖÖ³£¼ūµ„ÖŹĪŖµ»ĘÉ«·ŪÄ©£¬DµÄÄŚ²ć¹ģµĄČ«²æÅÅĀśµē×Ó£¬ĒŅ×īĶā²ćµē×ÓŹżĪŖl£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 ŅŃÖŖ»Æѧ·“Ó¦N2+3H22NH3µÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£ŗ
ŅŃÖŖ»Æѧ·“Ó¦N2+3H22NH3µÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | c£ØH+£© | B£® | $\frac{c£Ø{H}^{+}£©}{c£ØHF£©}$ | C£® | $\frac{c£Ø{F}^{-}£©}{c£Ø{H}^{+}£©}$ | D£® | $\frac{c£Ø{H}^{+}£©£®c£Ø{F}^{-}£©}{c£ØHF£©}$ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀĻĀ£¬a»ņbæÉŅŌÓėĖ®·¢Éś·“Ó¦ | |
| B£® | aÓėbÓƵ¼ĻßĮ¬½Ó²åČėH2SO4ÖŠ£¬ŌņŠĪ³ÉŌµē³ŲĒŅb¼«ÉĻÓŠH2·Å³ö | |
| C£® | aÓėbÓƵ¼ĻßĮ¬½Ó²åČėb£ØNO3£©2ÖŠŅ»¶Ø¹¹³ÉŌµē³Ų | |
| D£® | ÓƶčŠŌµē¼«µē½āa£ØNO3£©2Óėb£ØNO3£©2µÄ»ģŗĻŅŗ£¬ŌŚŃō¼«ĻČĪö³öb |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Cu2+”¢SO32-”¢OH- | B£® | Na+”¢H+”¢SO42- | C£® | OH-”¢Fe2+”¢SO42- | D£® | Na+”¢H+”¢CO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
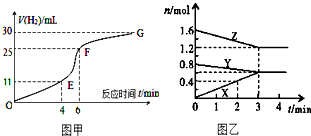 »Æѧ·“Ó¦ĖŁĀŹŗĶĻŽ¶ČŹĒ֊ѧ»ÆѧŌĄķÖŠŗÜÖŲŅŖ²æ·Ö£¬øł¾ŻĖłŃ§ÖŖŹ¶»Ų“šĻĀĮŠĪŹĢā£ŗ
»Æѧ·“Ó¦ĖŁĀŹŗĶĻŽ¶ČŹĒ֊ѧ»ÆѧŌĄķÖŠŗÜÖŲŅŖ²æ·Ö£¬øł¾ŻĖłŃ§ÖŖŹ¶»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com