
| A£®»ÆŗĻ·“Ó¦¶¼“󶹏Ē·ÅČČ·“Ó¦ |
| B£®·²ŹĒŠčŅŖ¼ÓČȵķ“Ó¦£¬¶¼ŹĒĪüČČ·“Ó¦ |
| C£®ĢåĻµµÄ»ģĀŅ¶ČŌö“óµÄ·“Ó¦¶¼ŹĒĪüČČ·“Ó¦ |
| D£®ÖŠŗĶ·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬Ęä»ÆѧÄÜæÉŅŌ×Ŗ»Æ³ÉµēÄÜ |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

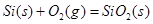 ;
;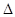 H="-989.2"
H="-989.2" 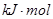
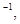 ŌņxµÄÖµĪŖ””””(”” ””)
ŌņxµÄÖµĪŖ””””(”” ””) | A£®460”” | B£®920 | C£®1 165.2”””” | D£®423.3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Q1<Q2 |
| B£®Éś³ÉĪļ×ÜÄÜĮæ¾łøßÓŚ·“Ó¦Īļ×ÜÄÜĮæ |
| C£®Éś³É1 mol HClĘųĢåŹ±·Å³öQ1ČČĮæ |
| D£®1 mol HBr(g)¾ßÓŠµÄÄÜĮæ“óÓŚ1 mol HBr(l)¾ßÓŠµÄÄÜĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
| A£®»Æѧ±ä»ÆÖŠµÄÄÜĮæ±ä»ÆÖ÷ŅŖÓÉ»Æѧ¼ü±ä»ÆŅżĘšµÄ |
| B£®·ÅČČ·“Ó¦·¢ÉśŹ±²»Ņ»¶ØŅŖ¼ÓČČ£¬µ«ĪüČČ·“Ó¦±ŲŠėŅŖ¼ÓČČ²ÅÄÜ·¢Éś |
| C£®øÖĢśµÄĪüŃõøÆŹ“ŗĶĪöĒāøÆŹ“µÄøŗ¼«·“Ó¦¶¼ĪŖFe”Ŗ2eŅ»= Fe2+ |
| D£®CaCO3(s) =" CaO(s)" + CO2(g) ¦¤H=" +" 178.5 KJ”¤mol-1µÄŅāŅåŹĒ±ķŹ¾1mol CaCO3ĶźČ«·Ö½āÉś³É1mol CaOŗĶ1mol CO2ĘųĢåŅŖ·Å³ö178.5 KJµÄČČĮæ |
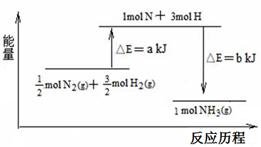
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
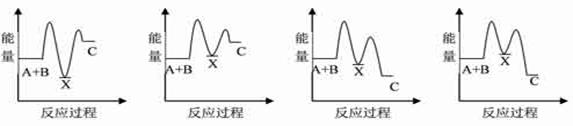
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®-1780kJ/mol | B£®-1220 kJ/mo | C£®-450 kJ/mol | D£®+430 kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
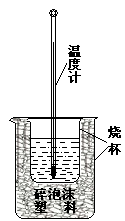
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®³£ĪĀĻĀ£¬ĪļÖŹµÄĮæÅØ¶Č¾łĪŖ0.1mol”¤L?1Na2CO3ŗĶNaHCO3µÄµČĢå»ż»ģŗĻČÜŅŗÖŠ£ŗ 2c(OH?)£2c(H+)£½3c(H2CO3)£«c(HCO3£)£c(CO32?) |
| B£®¦¤H£¼0,¦¤S£¾0µÄ·“Ó¦¶¼ŹĒ×Ō·¢·“Ó¦£¬¦¤H£¾0,¦¤S£¾0µÄ·“Ó¦ČĪŗĪĢõ¼ž¶¼ŹĒ·Ē×Ō·¢·“Ó¦£» |
| C£®ŅŃÖŖ£ŗP4(g)£«6Cl2(g)£½4PCl3(g) ¦¤H£½akJ”¤mol£1 P4(g)£«10Cl2(g)£½4PCl5(g)¦¤H£½bkJ”¤mol£1 P4¾ßÓŠÕżĖÄĆęĢå½į¹¹£¬PCl5ÖŠP£Cl¼üµÄ¼üÄÜĪŖckJ”¤mol£1,PCl3ÖŠP£Cl¼üµÄ¼üÄÜĪŖ1.2ckJ”¤mol£1£¬ÓÉ“Ė¼ĘĖćCl£Cl¼üµÄ¼üÄÜ 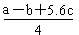 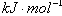 |
D£®ŌŚŅ»¶ØĪĀ¶ČĻĀ£¬¹Ģ¶ØĢå»żĪŖ2LĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦£ŗ2SO2(g)+O2(g) 2SO3(g) 2SO3(g) |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com