
【题目】合成药物异搏定路线中某一步骤如下:

X Y Z
下列说法不正确的是( )
A. 物质X中所有碳原子可能共平面
B. 可用FeCl3溶液鉴别Z中是否含有X
C. 等物质的量的X、Z分别与H2加成,最多消耗H2的物质的量之比为3∶5
D. 等物质的量的Y、Z分别与NaOH溶液反应,最多消耗NaOH的物质的量之比为1∶1
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列关于元素的叙述正确的是( )
A. 金属元素与非金属元素能形成共价化合物
B. 只有在原子中,质子数才与核外电子数相等
C. 目前使用的元素周期表中,最长的周期含有36种元素
D. 非金属元素形成的共价化合物中,原子的最外层电子数只能是2或8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】使1.0体积的某气态烷烃和烯烃的混合气体在足量空气中完全燃烧,生成2.0体积的二氧化碳和2.2体积的水蒸气(均在120℃、1.01×105Pa条件下测定),则混合气体中烷烃和烯烃的体积比为
A. 2:3 B. 1:4 C. 4:1 D. 3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有短周期主族元素X、Y、Z、R、T五种,R原子的最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Y与T同主族。五种元素原子半径与原子序数之间的关系如图所示。下列推断正确的是

A. 离子半径:Y<Z
B. 氢化物的稳定性:Y<T
C. 最高价氧化物对应水化物的酸性:T<R
D. 由X、Y、Z三种元素组成的常见化合物中含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100℃时,向容积为2L的密闭容器中充入一定量的X气体和Y气体,发生如下反应:X(g)+2Y(g) ![]() Z(g)反应过程中测定的部分数据见下表:
Z(g)反应过程中测定的部分数据见下表:
反应时间/min | n(X)/mol | n(Y)/ mol |
0 | 2.00 | 2.40 |
10 | 1.00 | |
30 | 0.40 |
下列说法正确的是
A. 前10 min内反应的平均速率为v(Z)=0.10 mol·L-1·min-1
B. 温度为200℃时,上述反应平衡常数为20,则正反应为吸热反应
C. 若密闭容器体积可变,其他条件不变,在达到平衡后缩小容器体积为原来一半,则c(X)<1mol/L
D. 保持其他条件不变,向容器中再充入1.00 mol X气体和1.20 mol Y气体,到达平衡后,X转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,在溶液中能够大量共存,当溶液中c(H+)=1×10-1mol·L-1时,有气体产生,而当溶液中c(H+)=1×10-13 mol·L-1时,又能生成沉淀。则该组离子可能为( )
A. HCO![]() 、Na+、Al3+、NO
、Na+、Al3+、NO![]() B. Fe2+、Na+、SO
B. Fe2+、Na+、SO![]() 、NO
、NO![]()
C. Mg2+、NH![]() 、SO
、SO![]() 、Cl- D. Na+、MnO
、Cl- D. Na+、MnO![]() 、NO
、NO![]() 、S2-
、S2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分,表中所列字母分别代表一种元素。
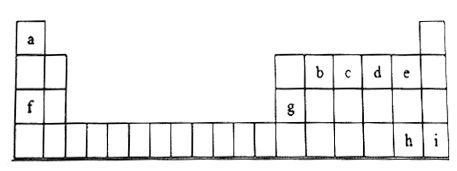
根据表格所给信息,回答下列问题:
(1)c元素原子的最高价氧化物对应的水化物的化学式___________(填化学式)
(2)b、c、d、e的原子半径依次_______(填“增大”或“减小”)
(3)e、h元素原子形成的氢化物中,热稳定性大的是__________(填氢化物的化学式)
(4)f、g元素的最高价氧化物对应水化物之间发生反应的化学方程式__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素的性质及其递变规律正确的是( )
A. 第二周期元素从左到右,最高正价从+1递增到+7
B. 同一主族的元素,原子半径越大,越容易失去电子,其单质的氧化性越强
C. 最外层电子数比次外层电子数多的元素一定位于第二周期
D. 碱金属元素是指ⅠA族的所有元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 乙酸、水、乙醇和金属钠反应剧烈程度,从剧烈到逐渐平缓
B. 淀粉和纤维素的组成可用(C6H10O5)n 表示,它们互为同分异构体
C. 硝酸不慎滴到皮肤上,发现皮肤变黄
D. 苯的结构式虽然用![]() 表示,但苯的结构却不是单、双键交替组成的环状结构,可以从它的邻二氯代物结构只有一种得到证明
表示,但苯的结构却不是单、双键交替组成的环状结构,可以从它的邻二氯代物结构只有一种得到证明
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com