
| ||
| ||
| ||
| 2.24g |
| 56g/mol |
| 0.64g |
| 16g/mol |


科目:高中化学 来源: 题型:
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2011-2012学年湖北武汉部分重点中学高一下学期期末考试化学题(带解析) 题型:填空题
(11分)地球上的资源是有限的,要合理的开发和利用。海水化学资源的利用具有非常广泛的前景。
I.下列有关海水综合利用的说法中,正确的是( )
A.海水中含有钾元素,只需经过物理变化就可以得到金属钾
B.用蒸馏、电渗析、离子交换等方法能从海水中提取淡水
C.从海水中可以得到氯化钠,电解熔融氯化钠可制取金属钠
D.利用潮汐发电是将化学能转化为电能
II.海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验: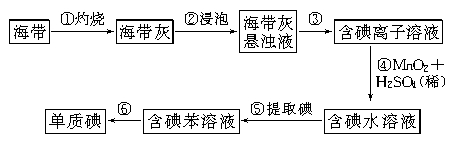
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是______________(从下列仪器中选出所需的仪器,用标号字母填写空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器 G.坩埚钳
(2)步骤③⑤的实验操作名称分别是______; ,步骤⑥的目的是从含碘的苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是________。
(3)步骤④反应的离子方程式是____________________________________________。
(4)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:
________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源:2014届湖北武汉部分重点中学高一下学期期末考试化学题(解析版) 题型:填空题
(11分)地球上的资源是有限的,要合理的开发和利用。海水化学资源的利用具有非常广泛的前景。
I.下列有关海水综合利用的说法中,正确的是( )
A.海水中含有钾元素,只需经过物理变化就可以得到金属钾
B.用蒸馏、电渗析、离子交换等方法能从海水中提取淡水
C.从海水中可以得到氯化钠,电解熔融氯化钠可制取金属钠
D.利用潮汐发电是将化学能转化为电能
II.海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:

请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是______________(从下列仪器中选出所需的仪器,用标号字母填写空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器 G.坩埚钳
(2)步骤③⑤的实验操作名称分别是______; ,步骤⑥的目的是从含碘的苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是________。
(3)步骤④反应的离子方程式是____________________________________________。
(4)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:
________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源:重庆市期末题 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com