
| A. | ②④⑥⑦ | B. | ③⑤⑥⑦ | C. | ④⑤⑥ | D. | ①②③ |
分析 ①浓盐酸随反应的进行浓度减小,当减小到一定浓度不再和二氧化锰反应.
②18.4mol/L的硫酸为浓硫酸,常温下遇到铁、铝金属发生的钝化,不再继续反应.
③向100mL3mol/L的硝酸中加入5.6g铁根据反应的量,铁全部反应生成二价铁离子和三价铁离子;
④合成氨的反应是可逆反应,不可能完全转化;
⑤将足量锌粉投入到50mL 18mol•L-1的硫酸中,首先生成二氧化硫,当浓硫酸转化为稀硫酸时与反应生成氢气,所以硫酸完全转化;
⑥将足量Ca(ClO)2投入到20mL 10mol•L-1盐酸中,发生归中反应生成氯气;
⑦将足量铜投入到50mL 12mol•L-1的硝酸中,首先生成二氧化氮,后来生成一氧化氮气体,硝酸完全转化.
解答 解:①浓盐酸浓度变稀到一定浓度不会和二氧化锰发生氧化还原反应,故错误;
②标准状况下,铝片遇浓硫酸发生钝化,阻止反应进行,故错误;
③根据反应Fe+4HNO3=Fe(NO3)3+NO+2H2O,0.3mol硝酸氧化0.075mol铁为三价铁离子,剩余0.025mol铁会继续和生成的0.1mol三价铁离子反应,依据反应2Fe3++Fe=3Fe2+ 可知剩余0.025mol铁全部溶解需要三价铁离子0.05mol,故正确;
④合成氨的反应是可逆反应,不可能完全转化,故错误;
⑤将足量锌粉投入到50mL 18mol•L-1的硫酸中,首先生成二氧化硫,当浓硫酸转化为稀硫酸时与反应生成氢气,所以硫酸完全转化,故正确;
⑥将足量Ca(ClO)2投入到20mL 10mol•L-1盐酸中,发生归中反应生成氯气,盐酸完全转化,故正确;
⑦将足量铜投入到50mL 12mol•L-1的硝酸中,首先生成二氧化氮,后来生成一氧化氮气体,硝酸完全转化,故正确;
故选B.
点评 本题考查氯气实验室制备中试剂的过程反应,常温下铝、铁在浓硫酸中钝化,变价金属铁与硝酸反应量不同产物不同及其有关过量计算方法,化学反应的可逆性,一定条件下达到平衡.注意审清题意,物质反应时条件不同产物不同,量不同产物不同.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:选择题
 将1molH2(g)和2mol I2(g)置于某2L密闭容器中,在一 定温度下发生反应:H2(g)+I2(g)?2HI(g)△H<0,并达到平衡,HI的体积分数ω(HI)随时间变化如曲线如图(Ⅱ)所示.若改变反应条件,ω(HI)的变化曲线如图(Ⅰ)所示,则改变的条件可能是( )
将1molH2(g)和2mol I2(g)置于某2L密闭容器中,在一 定温度下发生反应:H2(g)+I2(g)?2HI(g)△H<0,并达到平衡,HI的体积分数ω(HI)随时间变化如曲线如图(Ⅱ)所示.若改变反应条件,ω(HI)的变化曲线如图(Ⅰ)所示,则改变的条件可能是( )| A. | 恒温恒容加入适当催化剂 | B. | 恒温条件缩小体积 | ||
| C. | 恒容条件下升高温度 | D. | 恒温条件扩大反应容器 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 干冰用于人工降雨 | |
| B. | 蔗糖中加入浓硫酸,蔗糖变黑,体积膨胀 | |
| C. | 溶洞中钟乳石的形成 | |
| D. | 豆科作物的根瘤菌对空气中氮的固定 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
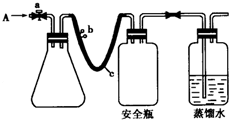 实验室用如图方法测定某水样中O2的含量.
实验室用如图方法测定某水样中O2的含量.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
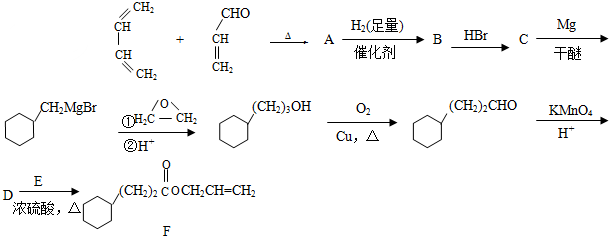
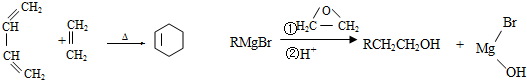
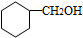 .
. .
. .
.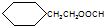
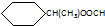 .
.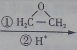 CH3CH2CH2CH2OH(其他试剂任选).
CH3CH2CH2CH2OH(其他试剂任选).查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | |||||||
| 3 | ① | ③ | ⑤ | ⑦ | ⑧ | ⑩ | ||
| 4 | ② | ④ | ⑨ |
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com