
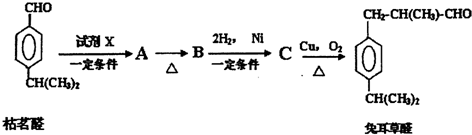


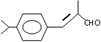
 ,B→C发生加成反应,C为
,B→C发生加成反应,C为 ,C→兔耳草醛发生醇的催化氧化反应;
,C→兔耳草醛发生醇的催化氧化反应; ,D→兔耳草醛发生加成反应,然后结合有机物的结构与性质来解答.
,D→兔耳草醛发生加成反应,然后结合有机物的结构与性质来解答. ,B→C发生加成反应,C为
,B→C发生加成反应,C为 ,C→兔耳草醛发生醇的催化氧化反应;
,C→兔耳草醛发生醇的催化氧化反应; ,D→兔耳草醛发生加成反应,
,D→兔耳草醛发生加成反应, ,含-CHO和碳碳双键,均能被强氧化剂氧化,而-CHO可被弱氧化剂氧化,则先加新制氢氧化铜悬浊液检验-CHO,酸化后利用溴水或高锰酸钾溶液检验碳碳双键,
,含-CHO和碳碳双键,均能被强氧化剂氧化,而-CHO可被弱氧化剂氧化,则先加新制氢氧化铜悬浊液检验-CHO,酸化后利用溴水或高锰酸钾溶液检验碳碳双键, ;新制氢氧化铜悬浊液;溴水或高锰酸钾溶液;
;新制氢氧化铜悬浊液;溴水或高锰酸钾溶液; ,故答案为:
,故答案为: ;
; ,D→兔耳草醛发生加成反应,故答案为:
,D→兔耳草醛发生加成反应,故答案为: ;加成反应;
;加成反应; 或
或 ,
, ;
; .
.


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
| A、FeSO4在反应中作氧化剂 |
| B、该反应在水溶液中进行 |
| C、Na2O2既是氧化剂又是还原剂 |
| D、Na2FeO4中铁元素+3价 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.2mol/L |
| B、4mol/L |
| C、5mol/L |
| D、6.25mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、其最高化合价为+3价 |
| B、可以形成化学式为KXO3的盐 |
| C、其氢化物可以用来做喷泉实验 |
| D、其最高价氧化物的水化物是强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂 |
| B、制取并用排水法收集氧气结束后,应立即停止加热 |
| C、浓NaOH溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液 |
| D、浓硫酸溅到皮肤上,立即用稀NaOH溶液洗涤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com