
科目:高中化学 来源: 题型:

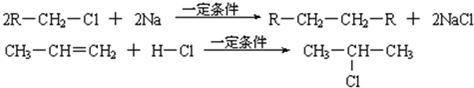
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
| 一定条件 |
| 一定条件 |
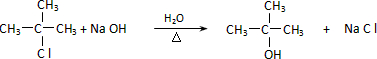

查看答案和解析>>
科目:高中化学 来源: 题型:
已知:(1)凡与醛基直接相连的碳原子上的氢原子称为αH原子,在稀酸或稀碱溶液的催化作用下(最常见的是稀碱催化剂),一分子醛上的αH?原子加成到另一分子醛的氧原子上,其余部分加成到羰基碳原子上生成β羟基醛,这个反应就叫做羟醛缩合,如
(1)
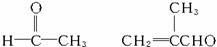
(2)2R—CH2Cl+2Na![]() R—CH2—CH2—R+2NaCl
R—CH2—CH2—R+2NaCl
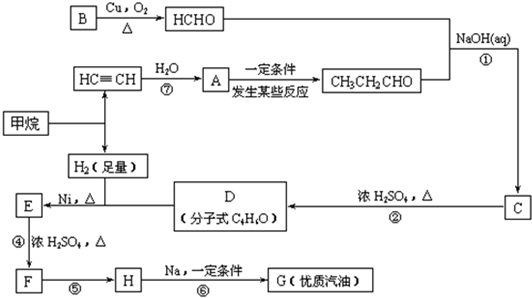
合成路线如下:
(1)写出下列物质的结构简式:A__________,D。__________
(2)写出合成路线中有关反应的反应类型:②__________,⑤__________。
(3)书写有关化学方程式:E![]() F:__________;
F:__________;
CH![]() G:__________。
G:__________。
(4)写出C的同分异构体的结构简式(且属于酯类的任意两种):__________、_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:(1)凡与醛基直接相连的碳原子上的氢称为αH原子,在稀碱溶液的催化作用下,一个醛分子上的αH原子连接到另一个醛分子的氧原子上,其余部分连接到羰基碳原子上生成羟基醛,如:
R—CH2—CHO+R1—CH2—CHO![]()

(2)2R—CH2—Cl+2Na![]() R—CH2—CH2—R+2NaCl
R—CH2—CH2—R+2NaCl
(3)CH3—CH=CH2+H—Cl![]()
![]()
合成路线如下:
(1)在反应②—⑦中,属于加成反应的是____________,属于消去反应的是____________。
(2)写出下列反应方程式
E![]() F:_________________________________________________________。
F:_________________________________________________________。
H![]() G:_________________________________________________________。
G:_________________________________________________________。
(3)H也能与NaOH溶液反应,其反应方程式为__________________,生成的有机物能否在Cu或Ag作催化剂的条件下被空气氧化__________(填“能”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:①凡与醛基直接相连的碳原子上的氢原子被称为α-H原子,在稀酸或稀碱溶液的催化作用下(最常见的是稀碱溶液催化剂),一分子醛上的α-H原子加成到另一分子醛的氧原子上,其余部分加成到羰基碳原子上生成β-羟基醛,这个反应就叫做羟醛缩合,如
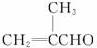
②2R—CH2Cl+2Na![]() R—CH2—CH2—R+2NaCl
R—CH2—CH2—R+2NaCl
合成路线如图1-6-6所示
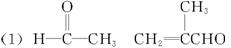
图1-6-6
(1)写出下列物质的结构简式:A___________,D___________。
(2)写出合成路线中有关的反应类型:②___________,⑤___________。
(3)书写有关化学反应方程式:
E→F:______________________;
CH3C(CH3)2Cl→G:___________。
(4)写出C的同分异构体的结构简式(且属于酯类的任意两种):___________、___________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年湖北省襄阳市高三调研三月统一测试理综化学试卷(解析版) 题型:填空题
(14分) 电池的发明和应用是化学家们对人类社会的重要贡献之一。
Ⅰ.每一次化学电池技术的突破,都带来了电子设备革命性的发展。最近,我国在甲醇燃料电池的相关技术上获得了新突破,原理如下图1所示。
(1)请写出从C口通入O2发生的电极反应式 。
(2)以石墨做电极电解饱和食盐水,如下图2所示。电解开始后在 的周围(填“阴极”或“阳极”)先出现红色。假设电池的理论效率为80%(电池的理论效率是指电池产生的最大电能与电池反应所释放的全部能量之比),若消耗6.4g甲醇气体,外电路通过的电子个数为 (保留两位有效数字,NA取6.02×1023)。

Ⅱ.随着电池使用范围的日益扩大,废旧电池潜在的污染已引起社会各界的广泛关注。
(1)电池生产企业排放的工业废水中常含有Cu2+等重金属离子,直接排放会造成污染,目前在工业废水处理过程中,依据沉淀转化的原理,常用FeS等难溶物质作为沉淀剂除去这些离子。已知室温下Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(CuS)=1.3×10-36mol2·L-2。请用离子方程式说明上述除杂的原理 。
(2)工业上为了处理含有Cr2O72-的酸性工业废水,用绿矾(FeSO4·7H2O)把废水中的六价铬离子还原成三价铬离子,再加入过量的石灰水,使铬离子转变为Cr(OH)3沉淀。
①氧化还原过程的离子方程式为 。
②常温下,Cr(OH)3的溶度积Ksp=1×10-32 mol4·L-4,溶液的pH至少为 ,才能使Cr3+沉淀完全。
③现用上述方法处理100m3含铬(+6价)78mg•L-1的废水,需用绿矾的质量为 kg。(写出主要计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com