
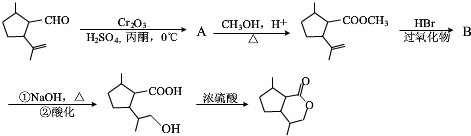
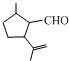
 µÄ·Ö×ÓŹ½ĪŖC10H16O£»Ęäŗ¬ÓŠµÄŗ¬Ńõ¹ŁÄÜĶÅĆū³ĘŹĒČ©»ł£®
µÄ·Ö×ÓŹ½ĪŖC10H16O£»Ęäŗ¬ÓŠµÄŗ¬Ńõ¹ŁÄÜĶÅĆū³ĘŹĒČ©»ł£®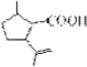 £®
£® £®Éś³ÉBĪļÖŹµÄ·“Ó¦ĄąŠĶĪŖ£ŗČ”“ś·“Ó¦£®
£®Éś³ÉBĪļÖŹµÄ·“Ó¦ĄąŠĶĪŖ£ŗČ”“ś·“Ó¦£®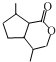 µÄĶ¬·ÖŅģ¹¹Ģå
µÄĶ¬·ÖŅģ¹¹Ģå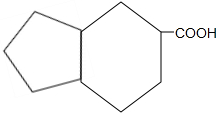 £®£ØČĪŠ“Ņ»ÖÖ£©
£®£ØČĪŠ“Ņ»ÖÖ£©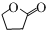 µÄŗĻ³ÉĀ·ĻßĶ¼£ØĪŽ»śŹŌ¼ĮČĪŃ”£©£¬ŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼ČēĻĀ£ŗ
µÄŗĻ³ÉĀ·ĻßĶ¼£ØĪŽ»śŹŌ¼ĮČĪŃ”£©£¬ŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼ČēĻĀ£ŗ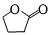
·ÖĪö ¶ŌÓ¦·“Ó¦Į÷³ĢÖŠÉę¼°ĪļÖŹµÄ½į¹¹¼ņŹ½æÉÖŖ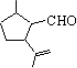 Ńõ»ÆÉś³ÉµÄAĪŖ
Ńõ»ÆÉś³ÉµÄAĪŖ £¬Óė¼×“¼·¢Éśõ„»Æ·“Ó¦£¬
£¬Óė¼×“¼·¢Éśõ„»Æ·“Ó¦£¬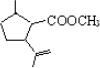 ÓėHBr·¢Éś·“Ó¦£¬½įŗĻBŗĶĒāŃõ»ÆÄĘ·“Ó¦µÄ²śĪļæÉÖŖBĪŖ
ÓėHBr·¢Éś·“Ó¦£¬½įŗĻBŗĶĒāŃõ»ÆÄĘ·“Ó¦µÄ²śĪļæÉÖŖBĪŖ £¬½įŗĻ¶ŌÓ¦ĪļÖŹµÄŠŌÖŹŅŌ¼°ĢāÄæŅŖĒó½ā“šøĆĢā£®
£¬½įŗĻ¶ŌÓ¦ĪļÖŹµÄŠŌÖŹŅŌ¼°ĢāÄæŅŖĒó½ā“šøĆĢā£®
½ā“š ½ā£ŗ¶ŌÓ¦·“Ó¦Į÷³ĢÖŠÉę¼°ĪļÖŹµÄ½į¹¹¼ņŹ½æÉÖŖ Ńõ»ÆÉś³ÉµÄAĪŖ
Ńõ»ÆÉś³ÉµÄAĪŖ £¬Óė¼×“¼·¢Éśõ„»Æ·“Ó¦£¬
£¬Óė¼×“¼·¢Éśõ„»Æ·“Ó¦£¬ ÓėHBr·¢Éś·“Ó¦£¬½įŗĻBŗĶĒāŃõ»ÆÄĘ·“Ó¦µÄ²śĪļæÉÖŖBĪŖ
ÓėHBr·¢Éś·“Ó¦£¬½įŗĻBŗĶĒāŃõ»ÆÄĘ·“Ó¦µÄ²śĪļæÉÖŖBĪŖ £¬
£¬
£Ø1£© µÄ·Ö×ÓŹ½ĪŖC10H16O£¬ŗ¬ÓŠµÄ¹ŁÄÜĶÅĪŖČ©»ł£¬¹Ź“š°øĪŖ£ŗC10H16O£»Č©»ł£»
µÄ·Ö×ÓŹ½ĪŖC10H16O£¬ŗ¬ÓŠµÄ¹ŁÄÜĶÅĪŖČ©»ł£¬¹Ź“š°øĪŖ£ŗC10H16O£»Č©»ł£»
£Ø2£©ÓÉŅŌÉĻ·ÖĪöæÉÖŖAĪŖ £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ £»
£»
£Ø3£© ÓėHBrŌŚ¹żŃõ»ÆĪļµÄ×÷ÓĆĻĀ·¢ÉśČ”“ś·“Ӧɜ³ÉµÄBĪŖ
ÓėHBrŌŚ¹żŃõ»ÆĪļµÄ×÷ÓĆĻĀ·¢ÉśČ”“ś·“Ӧɜ³ÉµÄBĪŖ £¬
£¬
·½³ĢŹ½ĪŖ £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ £»Č”“ś·“Ó¦£»
£»Č”“ś·“Ó¦£»
£Ø4£©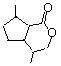
 £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ £»
£»
£Ø5£©CH2=CHCH2CHOŗĻ³É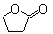
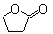
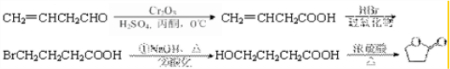 £¬
£¬
¹Ź“š°øĪŖ£ŗBrCH2CH2CH2COOH£»HOCH2CH2CH2COOH£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄŗĻ³É£¬°ŃĪÕĻ°ĢāÖŠµÄŠÅĻ¢ĶʶĻŗĻ³ÉĮ÷³ĢÖŠµÄĪļÖŹĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲŠÅĻ¢µÄÓ¦ÓĆ¼°ÖŖŹ¶ĒØŅĘÓ¦ÓĆÄÜĮ¦µÄ漲飬ĢāÄæÄѶČÖŠµČ£¬£Ø5£©ÖŠ½įŗĻŠÅĻ¢ŗĻ³ÉÓŠ»śĪļ£®


 ŠĀ»ĘøŌ±ų·ØĆܾķĻµĮŠ“š°ø
ŠĀ»ĘøŌ±ų·ØĆܾķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

| ·Šµć/”ę | ĆܶČ/£Øg•cm-3£© | Ė®ÖŠČܽāŠŌ | |
| Õż¶”“¼ | 11.72 | 0.8109 | Ī¢ČÜ |
| Õż¶”Č© | 75.7 | 0.8017 | Ī¢ČÜ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģ¼ĖįĒāÄĘČÜŅŗŗĶĻ”ŃĪĖį·“Ó¦£ŗCO32-+2H+ØTH2O+CO2”ü | |
| B£® | Ģ¼Ėį¼ŲČÜŅŗÓėĻ”ĮņĖį·“Ó¦£ŗCO32-+H+ØTCO2”ü+H2O | |
| C£® | ÄĘÓėĖ®·“Ó¦£ŗ2Na+2H2OØT2Na++2OH-+H2”ü | |
| D£® | ŹµŃéŹŅÖĘČ”ŃõĘų£ŗ2KClO3$\frac{\underline{\;MnO_{2}\;}}{”÷}$2K++2Cl-+3O2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1mol•L-1NaHCO3ČÜŅŗÖŠµÄNa+ŹżĪŖNA | |
| B£® | ³£ĪĀŹ±£¬4.4gCO2Ėłŗ¬µÄŃõŌ×ÓŹżĪŖ0.2NA | |
| C£® | 5.6g FeÓė×ćĮæĻ”ĻõĖį·“Ó¦£¬×ŖŅʵē×ÓŹżĪŖ0.2NA | |
| D£® | 1molNa ÓėO2 ·“Ӧɜ³ÉNa2O2ŗĶNa2Oµē×Ó×ŖŅĘŹżĪŖ0.1NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SO2ĶØČė¹żĮæµÄ°±Ė®ÖŠ£ŗSO2+NH3•H2OØTNH4++HSO3- | |
| B£® | FeOČÜÓŚ¹żĮæĻ”ĻõĖįÖŠ£ŗFeO+2H+ØTFe2++H2O | |
| C£® | NH4Al£ØSO4£©2ČÜŅŗÖŠ¼ÓČė¹żĮæNaOHČÜŅŗÖŠ£ŗNH4++Al3++4OH-ØTNH3•H2O+Al£ØOH£©3”ż | |
| D£® | ĶČÜÓŚĖį»ÆµÄH2O2ČÜŅŗÖŠ£ŗCu+H2O2+2H+ØTCu2++2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 £©¢Ü
£©¢Ü ¢ŻĘĻĢŃĢĒ¢Žµ°°×ÖŹ£®
¢ŻĘĻĢŃĢĒ¢Žµ°°×ÖŹ£®| A£® | ¢Ł¢Ū¢Ż | B£® | ¢Ś¢Ü¢Ž | C£® | ¢Ś¢Ū¢Ü | D£® | ¢Ł¢Ż¢Ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  µćČ¼Č÷¾«µĘ | B£® |  ³ĘĮæ10.05g¹ĢĢå | C£® |  ŅŗĢå¼ÓČČ | D£® |  Ēćµ¹ŅŗĢå |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com