
用FeCl3溶液腐蚀印刷电路板上的铜,所得的溶液中加入铁粉.对加入铁粉充分反应后的溶液分析合理的是( )
A.若无固体剩余,则溶液中一定有Fe3+
B.若有固体存在,则溶液中一定有Fe2+
C.若溶液中有Cu2+,则一定没有固体析出
D.若溶液中有Fe2+,则一定有Cu析出
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
如图甲所示,A河流经过某工业城市B。其中a处在上游,d处在下游。根据2009年市环保局监测站对A河流水质监测的结果,绘制成简图(如图乙所示)。
请根据图示回答:
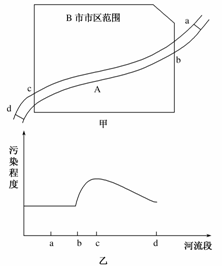
(1)造成A河流污染的主要污染源最可能分布在________河流段(用乙图中的英文字母表示)。
(2)列举造成A河流污染的三种可能污染源______________________________________________________________________________。
(3)对c处水样进行检测,发现其中含有Cu2+等重金属离子。若要把Cu2+变为单质铜回收,请用离子方程式或化学方程式表示两种回收的方法:
方法一:________________________________________________________________________________________________________________________________________________。
方法二:________________________________________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
分类思想是学习化学的重要思想,从分类的角度分析正确的是( )
A.SO2和NO2溶于水都显酸性,因而它们都是酸性氧化物
B.Na2O和NH3的水溶液均能导电,故均为电解质
C.Si和SiO2均属于原子晶体
D.Na2O和Na2O2与水反应均会生成强碱,故都是碱性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:还原性HSO3¯>I¯,氧化性IO3¯> I2 。在含3 mol NaHSO3的溶液中逐滴加入KIO3
溶液。加入KIO3和析出I2的物质的量的关系曲线如下图所示。下列说法不正确的是
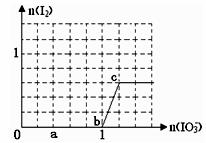
A.0~b间反应:3HSO3-+ IO3-= 3SO42-+ I-+ 3H+
B.a点时消耗NaHSO3的物质的量为1.2 mol
C.b~c间反应:I2仅是氧化产物
D.当溶液中I¯与I2的物质的量之比为5∶2时,加入的KIO3 为1.08mol
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现:在足量的稀氯
化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色。
(1)提出问题:Fe3+、Br2哪个氧化性更强?
(2)猜想:①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生氧化还原反应所致,则溶液呈黄色是含 (填化学式,下同)所致。
②乙同学认为氧化性:Br2>Fe3+,故上述现象是发生氧化还原反应所致,则溶液呈黄色是含 所致。
(3)设计实验并验证
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点是正确的。供选用的试剂:a、酚酞试液 b、CCl4 c、无水酒精 d、KSCN溶液。
请你在下表中写出丙同学选用的试剂及实验中观察到得现象。
| 选用试剂(填序号) | 实验现象 | |
| 方案1 | ||
| 方案2 |
(4)结论
氧化性:Br2>Fe3+。故在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生的离子反应方程式为 。
(5)实验后的思考
①根据上述实验推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是 。
②在100mLFeBr2溶液中通入2.24LCl2(标准状况),溶液中有1/2的Br-被氧化成单质Br2,则原FeBr2溶液的物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组气体中,在通常情况下既能用浓硫酸又能用碱石灰干燥的有( )
A.SO2、O2、N2 B.HCl、Cl2、CO2
C.CH4、H2、CO D.SO2、Cl2、O2
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器里放入四种物质,使其在一定条件下充分反应,测得数据如下:
| 四种物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 25 | 15 | 1 | 5 |
| 反应后质量(g) | 11 | 未测 | 1 | 22 |
则下列表述正确的是( )
A.该反应是复分解反应 B.丙一定是催化剂
C.乙全部发生了反应 D.甲与乙反应的质量比为14∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定质量的铁、氧化铁、氧化铜的混
合物粉末放入100mL 4.40 mol/L盐酸中,充分反应后产生896 mL H2(标准状况),残留固体1.28g。过滤,滤液中无Cu2+。将滤液加水稀释到200mL,测得其中c(H+)为0.400mol/L。则原混合物中单质铁的质量是
A.2.24g B.3.36g C.5.60g D.10.08g
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数,下列说法正确的是( )
A、30 g SiO2含有NA个Si-O共价键
B、1 L 0.2mol·L-1 Al2(SO4)3溶液中的离子总数为NA
C、标准状况下,22.4 L H2O所含原子个数大于3NA
D、含4 mol HCl的浓盐酸跟足量MnO2加热反应可制得Cl2的分子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com