
科目:高中化学 来源:2016-2017学年四川省高二10月月考化学卷(解析版) 题型:选择题
根据反应Br+H2 HBr+H的能量对反应历程的示意图甲进行判断,下列叙述中不正确的是( )
HBr+H的能量对反应历程的示意图甲进行判断,下列叙述中不正确的是( )
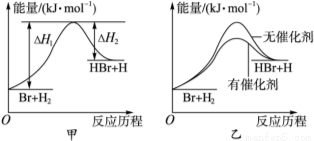
A.正反应吸热
B.加入催化剂,该化学反应的反应热不变
C.加入催化剂后,该反应的能量对反应历程的示意图可用图乙表示
D.加入催化剂可增大正反应速率,降低逆反应速率
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高二上期中化学卷(解析版) 题型:选择题
某物质的球棍模型如图所示,关于该物质的说法不正确的是( )
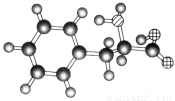
A.该物质的结构简式为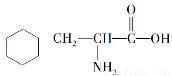
B.该 物质可以发生加成反应
物质可以发生加成反应
C.该物质既可以与强酸反应也可以与强碱反应
D.该物质可以聚合成高分子物质
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上期中化学卷(解析版) 题型:选择题
用0.2000 mol/L标准盐酸滴定待测烧碱的纯度,下列说法正确的是( )
A.滴定时可以用pH计或石蕊试液准确判断滴定终点
B.滴定前平视,滴定后俯视酸式滴定管,得出的滴定结果偏大
C.滴定前要用待测烧碱溶液洗涤锥形瓶
D.滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视锥形瓶内溶液颜色变化,直到滴定终点
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上期中化学卷(解析版) 题型:选择题
一种气态烷烃和一种气态烯烃的混合物9 g,其密度是相同条件下氢气目的的11.25倍。当混合气体通过足量的溴水时,溴水增重4.2 g,则这两种气态烃是( )
A.乙烷和乙烯 B.甲烷和丁烯 C.甲烷和丙烯 D.甲烷和乙烯
查看答案和解析>>
科目:高中化学 来源:2017届湖北省襄阳市四校高三上学期期中化学试卷(解析版) 题型:推断题
将晶体X加热分解,可得A、B、D、E、F和水六种产物,其中A、B、D都是中学化学中常见的氧化物,气体E是单质F所含元素的氢化物。
(1)A能溶于强酸、强碱,写出A与强碱溶液反应的离子方程式: 。
(2)B、D都是酸性氧化物且组成元素相同,B是形成酸雨的主要原因,B在一定条件下可以转化为D,则该方程式为 。已知煤燃烧所产生的烟气中含有B,若在煤中掺入适量生石灰,可减少B的排放,请写出其反应的化学方程式: 。
(3)E能使湿润的红色石蕊试纸变蓝,工业上常用E为原料制取硝酸,写出E催化氧化的化学方程式 ; E和氯气接触会产生白烟,该反应的化学方程式为 。
(4)由各分解产物的物质的量之比推测X的组成类似于明矾,则其化学式为 。
查看答案和解析>>
科目:高中化学 来源:2017届湖北省襄阳市四校高三上学期期中化学试卷(解析版) 题型:选择题
25°C时,某化学实验小组同学向用大理石和稀盐酸制备CO2后的残留液中滴加碳酸钠溶液,在溶液中插入pH传感器,测得pH变化曲线如图所示。下列说法不正确的是( )
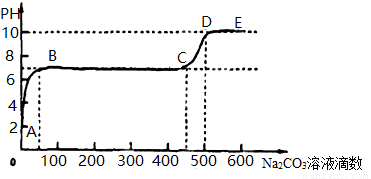
A.开始时溶液pH=2是因为残留液中还有盐酸剩余
B.BC段表示随着碳酸钠溶液的滴入,CaCO3沉淀的质量逐渐增加
C.滴入500滴碳酸钠溶液后溶液中c(OH-)>c(H+)
D.AB发生的反应为:Ca2+ + CO32-== CaCO3↓
查看答案和解析>>
科目:高中化学 来源:2017届广东省汕头市高三上期中化学试卷(解析版) 题型:选择题
高铁酸钾是一种高效绿色水处理剂,其工业制备的反应原理为:2Fe(OH)3 + 3KClO + 4KOH = 2K2FeO4 + 3KCl + 5H2O,下列说法正确的是
A.ClO ?做还原剂 B.Fe(OH)3在反应中被还原[
?做还原剂 B.Fe(OH)3在反应中被还原[
C .高铁酸钾中铁的化合价为+7 D.制备1molK2FeO4时转移3 mol 电子
.高铁酸钾中铁的化合价为+7 D.制备1molK2FeO4时转移3 mol 电子
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上期中化学试卷(解析版) 题型:填空题
将废旧锌锰电池处理得到含锰混合物,既能减少它对环境的污染,又能实现废电池的资源化利用。
Ⅰ. 回收二氯化锰:将废旧锌锰电池处理,得到含锰混合物,向该混合物加入浓盐酸并加热。
(1)写出MnO(OH)与浓盐酸反应的化学方程式:_________。
Ⅱ. 锰回收新方法:向含锰混合物加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止,其主要反应为:2MnOOH + MnO2 + 2H2C2O4 + 3H2SO4 == 3MnSO4 + 4CO2↑ + 6H2O
(2)与使用浓盐酸回收锰相比,新方法的优点是_________(答1点即可)。
(3)欲以MnSO4溶液为原料制备MnCO3,选用的加料方式___________(填字母),原因是___________。
已知:Ksp(MnCO3)=2.3×10﹣11、Ksp[Mn(OH)2]=2.1×10﹣13
a. 将MnSO4溶液与Na2CO3溶液同时加入到反应容器中
b. 将MnSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c. 将Na2CO3溶液缓慢加入到盛有MnSO4溶液的反应容器中
d. 以上三种方式都无法得到MnCO3.
Ⅲ. 现以含锰混合物为原料制备锰锌铁氧体的主要流程如图l所示:
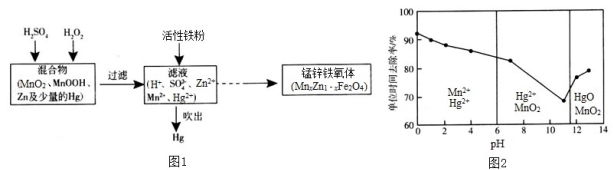
请回答下列问题:
(4)MnxZn1﹣xFe2O4中铁元素化合价为+3,则锰元素的化合价为___________。
(5)活性铁粉除汞时,铁粉的作用是_________(填“氧化剂”或“还原剂”)。
(6)酸浸时,MnO2与H2SO4、H2O2反应的离子方程式为__________________。
(7)除汞是以氮气为载气吹入滤液中,带出汞蒸气经KMnO4溶液进行吸收而实现的。在恒温下不同pH时,KMnO4溶液对Hg的单位时间去除率及主要产物如图2所示:
①写出pH=10时KMnO4溶液吸收汞蒸气的离子方程式________________。
②在强酸性环境中汞的单位时间去除率高,其原因除氢离子浓度增大使KMnO4溶液的氧化性增强外,还可能是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com