
����Ŀ��ҳ�����к��н϶�����飬�ɽ���ת��Ϊ���й�ҵ��ֵ����ϩ��
��1�� ������̼������������ϩ��
��C2H6��CO2�����ʵ���֮��Ϊ1��1ͨ�뷴Ӧ���У��������·�Ӧ��
����C2H6(g) ![]() C2H4(g) + H2(g) ��H1��+136.4 kJ��mol 1
C2H4(g) + H2(g) ��H1��+136.4 kJ��mol 1
����CO2(g) + H2(g) ![]() CO(g) + H2O(g) ��H2��+41.2 kJ��mol 1
CO(g) + H2O(g) ��H2��+41.2 kJ��mol 1
����C2H6(g) +CO2(g) ![]() C2H4(g) +CO(g) +H2O(g) ��H3
C2H4(g) +CO(g) +H2O(g) ��H3
������H1����H2������H3��______kJ��mol1��
�ڷ�Ӧ����C2H6(g) ![]() 2C(s)+3H2(g)Ϊ��̼��Ӧ�����ɵ�̼�����ڴ������棬 ���ʹ����Ļ��ԣ��ʵ�ͨ����� CO2 ������Ч�����̼����Ϸ���ʽ������ԭ��__��
2C(s)+3H2(g)Ϊ��̼��Ӧ�����ɵ�̼�����ڴ������棬 ���ʹ����Ļ��ԣ��ʵ�ͨ����� CO2 ������Ч�����̼����Ϸ���ʽ������ԭ��__��
�۶�����̼������������ϩ���о��ȵ�֮һ��ѡ���������ͬ��Ӧʱ�䣬��ͬ�¶ȡ���ͬ�������������±�����δ�ﵽƽ��״̬����

��ע��C2H4 ѡ���ԣ�ת����������������ϩ�İٷֱȡ�
CO ѡ���ԣ�ת���� CO2 ������ CO �İٷֱȡ�
�ԱȢ�͢÷�ӦӦ��ѡ��Ĵ���Ϊ__��������__��ʵ�������£�����������ʱ�����¶����ߣ�C2H6 ��ת�������ߣ��� C2H4 ��ѡ���Խ��ͣ�ԭ����__��
��2�� �������Ӵ���������������ؽ�����ת��Ϊ��ϩ��ʾ��ͼ��ͼ��
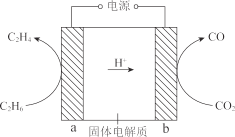
�ٵ缫 a ���Դ��______��������
�ڵ缫 b �ĵ缫��Ӧʽ�� ______��
���𰸡�+177.6 ����CO2������������ӦC+CO2 ![]() 2CO������C������CO2��������
2CO������C������CO2��������
Ӧ��������г̶����ӣ�������C2H6��Ũ�ȣ���Ӧ�����еij̶ȼ�С ���� ��ͬ�¶��£�����������ʱC2H6��ת���ʺ�C2H4��ѡ���Ծ��ϸ� �¶����ߣ���Ӧ�����������Ļ�ѧ��Ӧ���ʾ�����Ӧ������ĸ��� ���� CO2 +2e��+2H+=CO+H2O
��������
��1������֪��C2H6(g) ![]() C2H4(g) + H2(g) ��H1��+136.4 kJ��mol 1
C2H4(g) + H2(g) ��H1��+136.4 kJ��mol 1
����CO2(g) + H2(g) ![]() CO(g) + H2O(g) ��H2��+41.2 kJ��mol 1
CO(g) + H2O(g) ��H2��+41.2 kJ��mol 1
����C2H6(g) +CO2(g) ![]() C2H4(g) +CO(g) +H2O(g) ��H3
C2H4(g) +CO(g) +H2O(g) ��H3
�ɸ�˹���ɿ�֪����Ӧ��+��Ӧ���÷�Ӧ��������H3����H1+��H2=��+136.4 kJ��mol 1��+��+41.2 kJ��mol 1��=+177.6 kJ��mol 1���ʴ�Ϊ��+177.6��
�����������̼������������Ч�����̼��ԭ���ǣ�������̼����̼�ڼ��������·�Ӧ����һ����̼�����Ļ�̼����Ӧ�Ļ�ѧ����ʽΪC+CO2 ![]() 2CO�����������̼��������Ӧ����������Ӧ�����ƶ�����������ϵ��C2H6��Ũ�ȣ�ʹ��Ӧ�����淴Ӧ�����ƶ������ٻ�̼�����ɣ��ʴ�Ϊ������CO2������������ӦC+CO2
2CO�����������̼��������Ӧ����������Ӧ�����ƶ�����������ϵ��C2H6��Ũ�ȣ�ʹ��Ӧ�����淴Ӧ�����ƶ������ٻ�̼�����ɣ��ʴ�Ϊ������CO2������������ӦC+CO2 ![]() 2CO������C������CO2��������Ӧ��������г̶����ӣ�������C2H6��Ũ�ȣ���Ӧ�����еij̶ȼ�С��
2CO������C������CO2��������Ӧ��������г̶����ӣ�������C2H6��Ũ�ȣ���Ӧ�����еij̶ȼ�С��
���ɱ������ݿ�֪����ͬ�¶��£�����������ʱ��C2H6��ת���ʺ�C2H4��ѡ���Ծ��ϸߣ���ԱȢ�͢÷�ӦӦ��ѡ��Ĵ���Ϊ���Σ������¶ȣ���Ӧ�����������Ļ�ѧ��Ӧ���ʾ�����Ӧ���Ļ�ѧ��Ӧ��������ķ��ȸ�����C2H6 ��ת�������ߣ�C2H4��ѡ���Խ��ͣ��ʴ�Ϊ���¶����ߣ���Ӧ�����������Ļ�ѧ��Ӧ���ʾ�����Ӧ������ĸ��ࣻ
��2���ٵ����У��������������ƶ�����ͼ�������ӵ��ƶ������֪���缫 aΪ���������Դ�����������ʴ�Ϊ������
�ڵ����У��������������ƶ�����ͼ�������ӵ��ƶ������֪���缫bΪ�������������������£�������̼�������ϵõ��ӷ�����ԭ��Ӧ����һ����̼��ˮ���缫��ӦʽΪCO2 +2e��+2H+=CO+H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڻ�����2������ϩ��![]() ��������˵����ȷ����
��������˵����ȷ����
A. ����ʹϡ���������Һ��ɫ
B. ���Է����ӳɾۺϷ�Ӧ
C. ����������ԭ�ӹ�ƽ��
D. ������ˮ���ױ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������Դ�ǵ����о���һ���ȵ����⡣�����ѣ�CH3OCH3����δ������������ͺ�Һ������Ϊ�ྻҺ��ȼ��ʹ�ã���ҵ����CO��H2Ϊԭ������CH3OCH3����ҵ�Ʊ��������ڴ���Ӧ���У�ѹ��2.0��10.0Mpa���¶�230��280�棩�������з�Ӧ��
��CO(g)��2H2(g)![]() CH3OH(g) ��H1=-99kJ��mol-1
CH3OH(g) ��H1=-99kJ��mol-1
��2CH3OH(g)![]() CH3OCH3(g)��H2O(g) ��H2=-23.5kJ��mol-1
CH3OCH3(g)��H2O(g) ��H2=-23.5kJ��mol-1
��CO(g)��H2O(g)![]() CO2(g)��H2(g) ��H3=-41.2kJ��mol-1
CO2(g)��H2(g) ��H3=-41.2kJ��mol-1
��1������Ӧ���е��ܷ�Ӧ3CO(g)��3H2(g)![]() CH3OCH3(g)��CO2(g)��������H=___����Ӧԭ������ú����������֪�÷�Ӧ��ƽ�ⳣ������ʽΪK=
CH3OCH3(g)��CO2(g)��������H=___����Ӧԭ������ú����������֪�÷�Ӧ��ƽ�ⳣ������ʽΪK=![]() ��ÿ����1molH2��Ҫ����131.3kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ___��
��ÿ����1molH2��Ҫ����131.3kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ___��
��2���ڸ������£�����Ӧ�ٵ���ʼŨ�ȷֱ�Ϊ��c(CO)=0.6mol��L-1��c(H2)=1.4mol��L-1��8min��ﵽƽ�⣬CO��ת����Ϊ50%����8min��H2��ƽ����Ӧ����Ϊ___��
��3����t��ʱ����Ӧ�ڵ�ƽ�ⳣ��Ϊ400�����¶��£���1L���ܱ������м���һ���ļ״�����Ӧ��ijʱ�̲�ø���ֵ����ʵ���Ũ�����£�
���� | CH3OH | CH3OCH3 | H2O |
c(mol��L��1) | 0.46 | 1.0 | 1.0 |
��ʱ��v��___v������������������������������ƽ��ʱc(CH3OCH3)�����ʵ���Ũ����___��
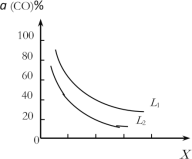
��4���ڣ�1��С���д���Ӧ�ҵ��ܷ�Ӧ3CO(g)��3H2(g)![]() CH3OCH3(g)��CO2(g)��CO��ƽ��ת����a(CO)���¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��ͼ��X����___�������¶�������ѹǿ��������L1___L2��������������������������
CH3OCH3(g)��CO2(g)��CO��ƽ��ת����a(CO)���¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��ͼ��X����___�������¶�������ѹǿ��������L1___L2��������������������������
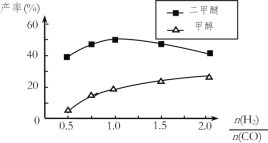
��5���ڴ�����������ͬʱ����������Ӧ������������ʼͶ�ϱ�![]() �ĸı�����Ѻͼ״��IJ��ʣ������е�̼ԭ��ռ��ʼCO��̼ԭ�ӵİٷ��ʣ�������ͼ�ı仯���ơ��Խ���Ͷ�ϱȴ���1.0֮������Ѳ��ʺͼ״����ʱ仯��ԭ��__��
�ĸı�����Ѻͼ״��IJ��ʣ������е�̼ԭ��ռ��ʼCO��̼ԭ�ӵİٷ��ʣ�������ͼ�ı仯���ơ��Խ���Ͷ�ϱȴ���1.0֮������Ѳ��ʺͼ״����ʱ仯��ԭ��__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�������е�һ����Ҫ��Ӧ��SO2��400~600 ���µĴ�������2SO2+O2![]() 2SO3������һ������Ӧ���ȵĿ��淴Ӧ�������Ӧ���ܱ������н��У������й�˵���д�����ǣ� ��
2SO3������һ������Ӧ���ȵĿ��淴Ӧ�������Ӧ���ܱ������н��У������й�˵���д�����ǣ� ��
A. ʹ�ô�����Ϊ�˼ӿ췴Ӧ���ʣ��������Ч��
B. �����������£�SO2������100%��ת��ΪSO3
C. Ϊ�����SO2��ת���ʣ�Ӧ�ʵ����O2��Ũ��
D. �ﵽƽ��ʱ��SO2��Ũ����SO3��Ũ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������軯�أ�K4[Fe(CN)6])˫�ƻ�Ѫ�Σ���һ����Ҫ�Ļ���ԭ�ϡ����������������ķ�ӦΪ��K4[Fe(CN)6]+FeCl3=KFe[Fe(CN)6]��(������) +3KCl���ش����⣺
(1)д����̬Fe3+�ĺ�������Ų�ʽ_________��
(2)K4[Fe(CN)6]�е������������ۼ��⣬����______��________������12mol ������K4[Fe(CN)6�����ʵ���Ϊ________mol��
(3)��Ѫ����Nԭ�ӵ��ӻ���ʽΪ______��C��N��O�ĵ�һ�������ɴ�С������Ϊ_____���縺���ɴ�С������Ϊ________��
(4)Fe��Na��K�ľ���ṹ��ͼ��ʾ��
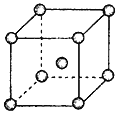
�� �Ƶ��۵�ȼظ��ߣ�ԭ����__________________________��
�� Feԭ�Ӱ뾶��r cm�������ӵ�����ΪNA���������ԭ������Ϊa���������ʵ��ܶ���_______g/cm3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ҫ������֮һ�������ɶ����ͷӾ��ಽ��Ӧ�ϳɣ��й������ֻ������˵������ȷ���ǣ� ��

A.�����£�1mol�����ͷ�ֻ����1molBr2��Ӧ
B.�����ͷӲ�����FeCl3��Һ������ɫ��Ӧ
C.1mol�������������3molH2�����ӳɷ�Ӧ
D.������KMnO4��Һ���ܼ������ͷӺ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���Ľṹ��ʽΪ![]() �����ڸ��л������������ȷ���ǣ� ��
�����ڸ��л������������ȷ���ǣ� ��
A. ����̼ԭ�ӿ��ܴ���ͬһƽ��
B. ���ڷ����廯�����ͬ���칹��������
C. �ܷ���ȡ����Ӧ��������Ӧ�ͼӳɷ�Ӧ
D. ��ʹ��ˮ������KMnO4��Һ��ɫ��ԭ����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�ݻ��ɱ���ܱ������м���WO3��H2���з�Ӧ��WO3(s)+3H2(g)![]() W(s)+3H2O(g)������˵������ȷ���ǣ� ��
W(s)+3H2O(g)������˵������ȷ���ǣ� ��
A.�������������Сһ�룬�䷴Ӧ��������
B.����������䣬����������䷴Ӧ���ʲ���
C.����ѹǿ���䣬����������H2O(g)��������������
D.����ѹǿ���䣬����������H2O(g)��H2(g)���������ʼ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(��ҪΪNO��NO2)�Ǵ�����Ⱦ������Ч�����������������Ⱦ��Ŀǰ��ѧ�����о����ȵ����⡣
��1��������[CO(NH2)2]���յ���������һ�ֿ��еķ�����
�������ڸ�����������NO2��Ӧת���������壬�÷�Ӧ�Ļ�ѧ����ʽΪ___����������ҺҲ�����յ�������о������������������![]() =1ʱ���ܵ���ԭ����ߣ����ţ�
=1ʱ���ܵ���ԭ����ߣ����ţ�![]() ��ֵ�����ܵ���ԭ�ʽ��͵���Ҫԭ����___��
��ֵ�����ܵ���ԭ�ʽ��͵���Ҫԭ����___��
����һ�����Ϊ1L�ĺ����ܱ������г���1molCO2��1molNH3���ں㶨�¶���ʹ�䷢����Ӧ2NH3(g)+CO2(g)![]() NH2CONH2(s)+H2O(g) ��H��0���ﵽƽ�⣬��������а��������������ʱ��ı仯��ͼ��ʾ��
NH2CONH2(s)+H2O(g) ��H��0���ﵽƽ�⣬��������а��������������ʱ��ı仯��ͼ��ʾ��
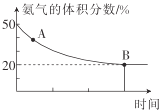
��A��ʱv��(CO2)___(������������������=��)B��ʱv��(CO2)��ԭ����___��B��ʱ��NH3��ת����Ϊ___��
�������йط�Ӧ2NH3(g)+CO2(g)![]() CO��NH2)2(s)+H2O(g)��˵����ȷ����___��
CO��NH2)2(s)+H2O(g)��˵����ȷ����___��
A.��������������أ�NH3��ת���ʽ�����
B.��Ӧ�ﵽƽ��ʱ�����ͷ�Ӧ��ϵ���¶ȣ�CO2��Ũ�ȼ�С
C.NH3��ת����ʼ�յ���CO2��ת����
D.������Ч�Ĵ����ܹ�������صIJ���
��2����֪O3���������������Ҫ��Ӧ���Ȼ�ѧ����ʽ���£�
2NO(g)+O2(g)=2NO2(g) ��H1=akJ��mol-1
NO(g)+O3(g)=NO2(g)+O2(g) ��H2=bkJ��mol-1
6NO2(g)+O3(g)=3N2O5(g) ��H3=ckJ��mol-1
��Ӧ4NO2(g)+O2(g)=2N2O5(g)��H=___(�ú�a��b��c�Ĵ���ʽ��ʾ)kJ��mol-1��
��3����������Ҳ���ü�Һ���ա���NO��NO2�Ļ�����屻NaOH��Һ��ȫ���գ�ֻ����һ���Σ�����εĻ�ѧʽΪ___����֪������Ka(HNO2)=5��10-4����ӦHNO2(aq)+NaOH(aq)![]() NaNO2(aq)+H2O(l)��ƽ�ⳣ��K=___��
NaNO2(aq)+H2O(l)��ƽ�ⳣ��K=___��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com