
【题目】下列物质中所含原子数目相等的是
A.34gH2O2和18gH2O B.2gO3和2gO2
C.5gCO和10gN2 D.1gH2和8gO2
【答案】B
【解析】
试题分析:A.34gH2O2的物质的量=![]() =1mol,含有原子物质的量=1mol×4=4mol,18gH2O的物质的量=
=1mol,含有原子物质的量=1mol×4=4mol,18gH2O的物质的量=![]() =1mol,含有原子物质的量=1mol×3=3mol,二者含有原子数目不相等,故A错误;B.O3和O2都由O原子构成,二者质量相等,含有O原子数目相等,故B正确;C.CO和N2都是双原子分子,二者摩尔质量相等,质量不相等,故二者物质的量不相等,含有原子数目不相等,故C错误;D.1gH2的物质的量=
=1mol,含有原子物质的量=1mol×3=3mol,二者含有原子数目不相等,故A错误;B.O3和O2都由O原子构成,二者质量相等,含有O原子数目相等,故B正确;C.CO和N2都是双原子分子,二者摩尔质量相等,质量不相等,故二者物质的量不相等,含有原子数目不相等,故C错误;D.1gH2的物质的量=![]() =0.5mol,含有原子物质的量=0.5mol×2=1mol,8gO2的物质的量=
=0.5mol,含有原子物质的量=0.5mol×2=1mol,8gO2的物质的量=![]() =0.25mol,含有原子物质的量=0.25mol×2=0.5mol,二者含有原子数目不相等,故D错误,故选B。
=0.25mol,含有原子物质的量=0.25mol×2=0.5mol,二者含有原子数目不相等,故D错误,故选B。


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
【题目】盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现就三大酸与金属铜反应的情况,回答下列问题:
(1)稀盐酸不与Cu 反应,若在稀盐酸中加入H2O2后,则可使铜顺利溶解。该反应的化学方程式为:___________________。
(2)在一定体积的10mol/L的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol。则浓硫酸的实际体积__________(填“大于”、“ 等于”或“小于”)180mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为________________。
(3)镁铁混合物4.9g,溶解在过量的某浓度的稀硝酸中,完全反应后得到标准状况下2 .24LNO气体。若向反应后的溶液中加入足量的烧碱,则可生成沉淀的质量是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,22.4LCl2和HCl的混合气体所含分子总数为2NA
B.常温常压下,18 g H2O中含有的原子总数为3 NA
C.标准状况下,11.2 L CH3CH2OH中含有的分子数目为0.5 NA
D.1 L 0.1 mol/L NaOH溶液含有阴阳离子总数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学研究发现,苹果含有微量元素Zn,而锌是构成与记忆力息息相关的核酸和蛋白质不可缺少的元素。儿童缺锌就会导致大脑发育不良,因此苹果又被称为记忆之果。这说明无机盐离子
A. 对维持酸碱平衡有重要作用
B. 对维持细胞形态有重要作用
C. 对调节细胞内的渗透压有重要作用
D. 对维持生物体的生命活动有重要作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,10 mL 0.40 mol·L-1 H2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表。下列叙述不正确的是(溶液体积变化忽略不计)( )
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
A.0~6 min的平均反应速率:v(H2O2)≈3.3×10-2mol·(L·min)-1
B.6~10 min的平均反应速率:v(H2O2)<3.3×10-2mol·(L·min)-1
C.反应至6 min时,c(H2O2)=0.30 mol·L-1
D.反应至6 min时,H2O2分解了50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产和生活密切相关。下列过程中没有发生化学变化的是( )
A.氯气作水杀菌消毒剂
B.硅胶作袋装食品的干燥剂
C.二氧化硫作纸浆的漂白剂
D.肥皂水作蚊虫叮咬处的清洗剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中A~H均为中学化学中常见的物质,A、B、H是气体,它们之间有如下转化关系(反应中生成的水已略去)。
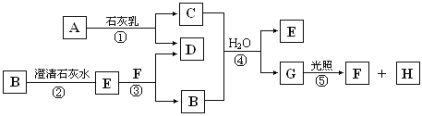
请回答以下问题:
(1)E是 (填化学式),G是 (填名称);
(2)C物质在日常生活中可作 ;
(3)写出反应①的化学方程式 ;
C与浓盐酸反应,可以生成A气体,写出反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________。
(2)①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ΔH4=-1048.9kJ/mol
上述反应热效应之间的关系式为ΔH4=__________,联氨和N2O4可作为火箭推进剂的主要原因为______________。
(3)联氨为二元弱碱,在水中的电离方式与氨相似,联氨第一步电离方程式为:_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com