
【题目】(13分)由乙烯和其它无机原料合成环状酯E和高分子化合物H的示意图如下:

请回答下列问题:
(1)写出结构简式:A F C
(2)反应类型:X 、Y
(3)写出化学反应方程式:
A→B
G→H
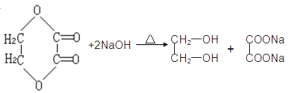
(4)若环状酯E在NaOH溶液中共热,则发生反应的化学方程式为:
【答案】(1)A:CH2BrCH2Br F:CH≡CH, C:OHC—CHO(每空1分)
(2)X:酯化反应 Y:加聚反应 (3)A→B:![]()
G→H:![]()
【解析】乙烯含有碳碳双键,能和溴水发生加成反应,生成1,2-二溴乙烷,即A的结构简式为CH2BrCH2Br。A在氢氧化钠的醇溶液中发生消去反应生成F,则F是乙炔。乙炔和氯化氢发生加成反应生成G,则G是CH2=CHCl。G中含有碳碳双键,能发生加聚反应生成高分子化合物H,则H是聚氯乙烯。A也能在氢氧化钠的水溶液中发生水解生成B,则B是乙二醇。乙二醇氧化生成C,则C是乙二醛。乙二醛继续被氧化生成乙二酸。乙二酸和乙二醇发生酯化反应生成环酯E。


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】聚酯增塑剂广泛用于耐油电缆、煤气管、防水卷材、鞋料、室内高级装饰品、耐油耐汽油的特殊制品等。聚酯增塑剂G及某医药中间体N的一种合成路线如下(部分反应条件略去):

已知:
(1)
(2)CH3CH=CHCH2CH3![]() CH3COOH+CH3CH2COOH
CH3COOH+CH3CH2COOH
请回答下列问题:
(1)N中官能团的名称为________;反应②的试剂和条件是:__________;
(2)反应⑤的反应类型是________,反应⑧的反应类型是____________;
(3)I的结构简式为____________;
(4)写出B与H反应生成聚酯增塑剂G的化学方程式__________;
(5)H的同分异构体满足下列条件的共有______种(不含立体异构)
①1mol该物质能与2molNaOH溶液反应
②1mol该物质与银氨溶液反应生成4molAg
③有且只有2个甲基
其中核磁共振氢谱显示位组峰,且峰面积比为3:1:2的是________(写出一种结构简式)
(6)参考以上合成路线的信息,设计一条以苯甲酸和乙醇为原料合成![]() 的路线(无机试剂任选,需注明反应条件):_________。
的路线(无机试剂任选,需注明反应条件):_________。
示例:原料![]() …产物
…产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用接触法制5t98%的浓硫酸,在理论上需要含FeS2 75%(杂质不含硫元素)的硫铁矿为 ( )
A. 4.3t B. 8t C. 4t D. 5.6t
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性锌锰电池是日常生活中消耗量最大的电池,其构造如图所示。
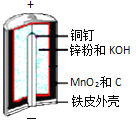
放电时总反应为:Zn + 2H2O + 2MnO2![]() Zn(OH)2 + 2MnOOH
Zn(OH)2 + 2MnOOH
从废旧碱性锌锰电池中回收Zn和MnO2的工艺如下:
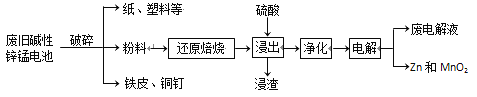
回答下列问题:
(1)MnOOH中,Mn元素的化合价为________。
(2)“还原焙烧”过程中,高价金属化合物被还原为低价氧化物或金属单质(其中MnOOH、MnO2被还原成MnO),主要原因是“粉料”中含有________。
(3)“净化”是为了除去浸出液中的Fe2+,方法是:加入________(填化学式)溶液将Fe2+氧化为Fe3+,再调节pH使Fe3+完全沉淀。(离子浓度小于1×10-5mol·L-1即为沉淀完全)已知浸出液中Mn2+、Zn2+的浓度约为0.1 mol·L-1,根据下列数据计算调节pH的合
理范围是________至________。
化合物 | Mn(OH)2 | Zn(OH)2 | Fe(OH)3 |
KSP近似值 | 10-13 | 10-17 | 10-38 |
(4)“电解”时,阳极的电极反应式为_____。本工艺中应循环利用的物质是_____(填化学式)。
(5)若将“粉料”直接与盐酸共热反应后过滤,滤液的主要成分是ZnCl2和MnCl2。“粉料”中的MnOOH与盐酸反应的化学方程式为________。
(6)某碱性锌锰电池维持电流强度0.5A(相当于每秒通过5×10-6 mol电子),连续工作80分钟即接近失效。如果制造一节电池所需的锌粉为6 g,则电池失效时仍有________%的金属锌未参加反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是()
A. 2015年8月12日,天津滨海新区某公司的仓库发生爆炸,事发仓库里存放了大量的硝酸铵、氰化钠、电石和金属钠等危险化学品这四种药品均属于电解质
B. 纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应
C. 氮氧化物对环境有很大危害,如破坏臭氧层,形成酸雨,产生光化学烟雾等
D. 工业上利用氯气与澄清石灰水反应制取漂白粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、社会发展等息息相关。下列说法正确的是( )
A. 做衣服的棉、麻、丝绸灼烧有烧焦羽毛的气味
B. 糖尿病人应少吃含糖类的食品,可常喝糯米八宝粥
C. 现代工业生产中的芳香烃来源于石油的催化重整和煤的干馏
D. 豆浆中富含大豆蛋白,煮沸后蛋白质即水解生成氨基酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化硼的熔点为-107.3 ℃,沸点为12.5 ℃,易水解生成硼酸(H3BO3),可用于制造高纯硼、有机合成催化剂等。实验室制取三氯化硼的原理为B2O3+3C+3Cl2![]() 2BCl3+3CO。
2BCl3+3CO。
(1)甲组同学拟用下列装置制取纯净干燥的氯气(不用收集)。

①装置B中盛放的试剂是__,装置C的作用是___________________。
②装置A中发生反应的离子方程式为 _____________________________。
(2)乙组同学选用甲组实验中的装置A、B、C和下列装置(装置可重复使用)制取BCl3并验证反应中有CO生成。
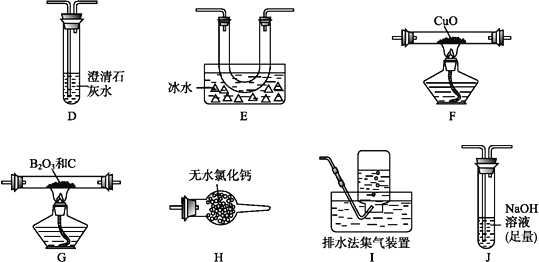
①乙组同学的实验装置中,依次连接的合理顺序为
A→B→C→G→__→__→__→__→F→D→I。
②能证明反应中有CO生成的现象是___________________________。
③开始实验时,先点燃____(填“A” 或“G”)处的酒精灯。
④请写出BCl3水解的化学方程式__________________________。
⑤硼酸是一元弱酸,其钠盐化学式为Na [B(OH)4],则硼酸在水中电离方程式是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.写出下列反应的离子方程式:
(1)将鸡蛋壳在醋酸中溶解有气泡产生:_____________________________________________;
(2)CuSO4溶液与Ba(OH)2溶液混合:________________________________________。
Ⅱ.对一份稀溶液作初步分析后发现,溶液无色、澄清,其可能含有![]() 、Na+、
、Na+、![]() 、H+、
、H+、![]() 、
、![]() 、Cl等离子中的若干种。然后又作了如下分析,以确定这些离子是否存在。
、Cl等离子中的若干种。然后又作了如下分析,以确定这些离子是否存在。
①用石蕊试液检测该溶液时,溶液显红色。
②取2 mL溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。
请回答下列问题:
(1)原溶液中一定存在的离子是__________,一定不存在的离子是____________。
(2)在上述实验操作中,有错误的步骤是(填代号)______。对该错误改正的方法是(要作较详细的说明)_________________________________________________________。
(3)到目前为止,不能肯定在原溶液中是否存在的离子是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是 ( )
A. 1mol NaCl分子中含有1mol Na+和1mol Cl-
B. 离子化合物和共价化合物溶于水都能导电
C. 离子键的形成一定有电子的得失
D. KOH溶于水电离出K+ 和OH- 不是化学变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com