
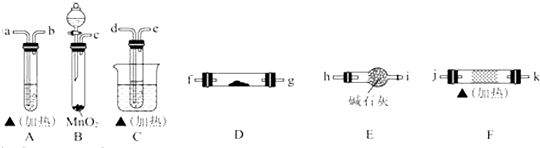
分析 (1)用B发生制取氧气,产生的氧气中含有水蒸气,所以需要干燥装置,则应选择装置E,乙醇的催化氧化实验,需产生乙醇蒸气,则应选择装置C,无水乙醇与氧气发生催化氧化,则应选择装置F,验证生成的水,则应选择装置D,验证乙醛,则应选择装置A,据此连接装置;
(2)B中过氧化氢在二氧化锰催化作用下生成水和氧气;
(3)F装置为乙醇催化氧化,乙醇在铜做催化剂条件下发生催化氧化,催化氧化的产物为乙醛;
乙醇催化氧化是一个放热反应,该反应引发后,不需加热即可进行,所以撤掉酒精灯后铜丝保持红热;
(4)乙醛能和氢氧化铜悬浊液反应,生成砖红色沉淀;装置D的作用是检验水蒸气,药品为白色的无水硫酸铜粉末,无水硫酸铜与水反应生成蓝色的五水硫酸铜;
(5)C装置是为乙醇催化氧化提供乙醇蒸气,所以为了得到平稳气流,且节约能源,改进C装置,需使用温度计,控制C装置中水浴的温度略高于乙醇沸点.
解答 解:(1)用B发生制取氧气,产生的氧气中含有水蒸气,所以需要干燥装置,则应选择装置E,乙醇的催化氧化实验,需产生乙醇蒸气,则应选择装置C,无水乙醇与氧气发生催化氧化,则应选择装置F,验证生成的水,则应选择装置D,验证乙醛,则应选择装置A,所以按气流方向连接顺序为:c→hi→de→jk(或kj)→fg(或gf)→a;
故答案为:c→hi→de→jk(或kj)→fg(或gf)→a;
(2)过氧化氢在二氧化锰催化作用下生成水和氧气,化学方程式:2H2O2$\frac{\underline{\;二氧化锰\;}}{\;}$2H2O+O2↑,故答案为:2H2O2$\frac{\underline{\;二氧化锰\;}}{\;}$2H2O+O2↑;
(3)F装置为乙醇催化氧化,乙醇催化氧化的产物为乙醛,反应方程式为:2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O,所以F装置中的固体试剂是铜丝,乙醇催化氧化是一个放热反应,该反应引发后,不需加热即可进行,所以撤掉酒精灯后铜丝保持红热;
故答案为:铜丝;2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O;该反应为放热反应,反应过程放出的热量能维持反应继续进行;
(4)乙醛能和氢氧化铜悬浊液反应,生成砖红色沉淀,所以A中会产生红色沉淀,装置D的作用是检验水蒸气,药品为白色的无水硫酸铜粉末,发生反应为:CuSO4+5H2O═CuSO4•5H2O,无水硫酸铜变蓝说明混合气体中有水蒸气;
故答案为:A中出现砖红色沉淀、D中白色粉末变为蓝色;
(5)C装置是为乙醇催化氧化提供乙醇蒸气,所以为了得到平稳气流,且节约能源,改进C装置,需使用温度计,控制C装置中水浴的温度略高于乙醇沸点;
故答案为:使用温度计,控制C装置中水浴的温度略高于乙醇沸点.
点评 本题考查了乙醇的催化氧化实验,明确乙醇结构及性质是解题关键,题目难度中等.


 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:选择题
| A. | 该消毒液的pH约为13:ClO-+H2O?HClO+OH- | |
| B. | 该消毒液可用NaOH溶液吸收Cl2制备:Cl2+2OH-═Cl-+ClO-+H2O | |
| C. | 该消毒液与洁厕灵(主要成分为HCl)混用,产生Cl2:2H++Cl-+ClO-═Cl2↑+H2O | |
| D. | 该消毒液加白醋生成HClO,可增强漂白作用:CH3COOH+ClO-═HClO+CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 萃取操作时,在选择萃取剂时,要求萃取剂和原溶剂不互溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 实验目的 | 实验操作 | |
| A | 鉴别Al3+和Fe3+ | 分别加入少量NaOH溶液 |
| B | 比较Fe和Cu的金属活动性 | 分别加入浓硝酸 |
| C | 证明品红溶液褪色的原因是通入了SO2 | 将褪色后的溶液再加热 |
| D | 分离乙酸乙酯和乙酸 | 加饱和NaOH溶液,蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
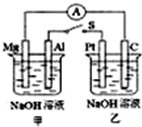
| A. | 电流表指针不发生偏转 | |
| B. | Al、Pt两极有H2产生 | |
| C. | Mg、C两极生成的气体可以恰好完全反应 | |
| D. | 甲池pH减小,乙池pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 主要实验步骤及实验现象 |
| ① | 在含Y的溶液中,加入稀硫酸放置,产生浅黄色沉淀和无色有刺激性气味的气体,该气体可使品红溶液褪色 |
| ② | 在含Z的溶液中,滴加盐酸,开始有白色沉淀,继续滴加盐酸,白色沉淀先增加后消失,然后加入过量的氨水又出现白色沉淀 |
| ③ | 将实验②最终得到的混合物加热蒸发、灼烧,最终得到白色固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | C═C | C-C | C≡C | C-H |
| E/(kJ•mol-1) | 436.0 | 615 | 347.7 | 812 | 413.4 |

 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
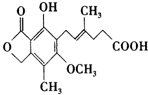 ,下列有关麦考酚酸说法不正确的是( )
,下列有关麦考酚酸说法不正确的是( )| A. | 分子式为C17H20O6 | |
| B. | 能与FeCl3溶液显色,与浓溴水反应,最多消耗量1 mol Br2 | |
| C. | 1mol麦考酚酸最多与3 mol NaOH反应 | |
| D. | 在一定条件下可发生加成,加聚,取代,消去四种反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com