
CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法正确的是
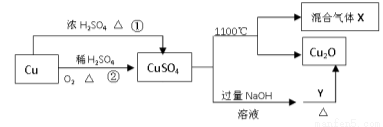
A.途径①和途径②都体现了硫酸的酸性和氧化性
B.Y可以是酒精溶液
C.CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体
D.将CuSO4溶液蒸发浓缩、冷却结晶,可制得胆矾晶体
D
【解析】
试题分析:A.在Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O,中硫酸表现氧化性和酸性;在2Cu+O2+ 2H2SO4
CuSO4+SO2↑+2H2O,中硫酸表现氧化性和酸性;在2Cu+O2+ 2H2SO4 2CuSO4+2H2O中硫酸表现酸性,二者的作用性质不同,错误;B.在CuSO4溶液中加入过量的NaOH溶液,发生复分解反应:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;新制Cu(OH)2与乙醛在加热时发生反应产生Cu2O,错误;C.CuSO4在1100℃分解产生Cu2O,Cu元素的化合价降低,根据氧化还原反应中电子转移数目可知应该有元素的化合价升高的,因此所得气体X可能含有O2,因此不可能是酯含有SO2和SO3,错误;D.将CuSO4溶液蒸发浓缩、冷却结晶,可制得胆矾晶体,正确。
2CuSO4+2H2O中硫酸表现酸性,二者的作用性质不同,错误;B.在CuSO4溶液中加入过量的NaOH溶液,发生复分解反应:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;新制Cu(OH)2与乙醛在加热时发生反应产生Cu2O,错误;C.CuSO4在1100℃分解产生Cu2O,Cu元素的化合价降低,根据氧化还原反应中电子转移数目可知应该有元素的化合价升高的,因此所得气体X可能含有O2,因此不可能是酯含有SO2和SO3,错误;D.将CuSO4溶液蒸发浓缩、冷却结晶,可制得胆矾晶体,正确。
考点:考查CuSO4的性质、应用的知识。


 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源:2015届河南省10月联考化学试卷(解析版) 题型:填空题
(10分)1 000 mL某待测液中除含有0.2 mol/L的Na+外,还可能含有下列离子中的一种或多种:
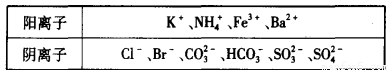
现进行如下实验操作(每次实验所加试剂均过量):
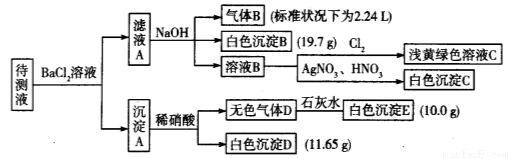
(1)写出生成白色沉淀B的离子方程式:___________________________________________。
(2)待测液中肯定不存在的阳离子是_________________。
(3)若无色气体D是单一气体:
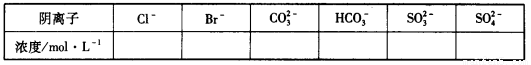
①将阴离子的物质的量浓度填入下表中(一定不存在的填“0”,不能确定的填“?”):
②判断原溶液中K+是否存在,若存在,求其物质的量浓度的最小值,若不存在,请说明理由:_______________________________________________________________________________。
(4)若无色气体D是混合气体:
①待测液中一定含有的阴离子是____________________________。
②沉淀A中能与稀硝酸反应的成分是______________________________(写化学式)。
查看答案和解析>>
科目:高中化学 来源:2015届河南省洛阳市高三上学期期中考试化学试卷(解析版) 题型:选择题
相同物质的量的H2O和H2相比,下列说法不正确的是
A.物质的质量之比为9:1 B.原子数之比为1:1
C.分子数之比为1:1 D.电子数之比为5:1
查看答案和解析>>
科目:高中化学 来源:2015届河南省高三9月第二次阶段考化学试卷(解析版) 题型:选择题
下列表示对应化学反应的离子方程式正确的是( )
A.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O=3I2+6OH-
B.向NH4HCO3溶液中加过量NaOH溶液并加热:NH4++OH-  NH3↑+H2O
NH3↑+H2O
C.将过量二氧化硫气体通入冷氨水中:SO2+NH3?H2O =HSO3-+NH4+
D.用稀硝酸洗涤试管内壁的银镜:Ag+2H++3NO3-=Ag++NO↑+H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省高三上学期期中理综化学试卷(A)(解析版) 题型:填空题
[化学——选修5:有机化学基础](15分)
阿托酸乙酯可用于辅助胃肠道痉挛及溃疡。阿托酸乙酯的一种合成路线如下图所示:

请回答下列问题:
(1)E的分子式为 ,F的结构简式 ,阿托酸乙酯所含官能团的名称 ;
(2)在反应①②③④⑤⑥⑦⑧中,属于取代反应的有 ;
(3)反应③的方程式 。
(4)有关阿托酸乙酯的说法正确的是
A.能使高锰酸钾褪色,不能使溴水褪色
B.1mol阿托酸乙酯最多能与4molH2加成
C.能发生加成、加聚、氧化、水解等反应
D.分子式为C11H13O2
(5)D的同分异构体有多种,符合含有苯环且能与碳酸氢钠反应放出气体的同分异构体有 种(不包含D)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省高三上学期期中理综化学试卷(A)(解析版) 题型:选择题
下列离子组中所给离子在水溶液中能大量共存,且当加入试剂后反应的离子方程式书写完全且正确的是
选项 | 离子组 | 加入试剂 | 发生反应的离子方程式 |
A | Fe3+、S2ˉ、Clˉ、Na+ | NaOH溶液 | Fe3++3OHˉ=Fe(OH)3↓ |
B | Na+、Al3+、Clˉ、SO42ˉ | 少量KOH溶液 | Al3++3OHˉ=Al(OH)3↓ |
C | H+、Fe2+、SO42ˉ、NO3ˉ | BaCl 2溶液 | SO42ˉ+Ba2+=BaSO4↓ |
D | Na+、K+、ClOˉ、SO42ˉ | 通入少量SO2 | 2ClOˉ+SO2+H2O=2HClO+SO32ˉ |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高三上学期第四次检测化学试卷(解析版) 题型:选择题
在1100 ℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g)  Fe(s)+CO2(g) ΔH=a kJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是
Fe(s)+CO2(g) ΔH=a kJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是
A.若生成1 mol Fe,则吸收的热量小于a kJ
B.若升高温度,正反应速率加快,逆反应速率减慢,则化学平衡正向移动
C.若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态
D.达到化学平衡状态时,若c(CO)=0.100 mol/L,则c(CO2)=0.0263 mol/L可将气体顺利排出
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高三上学期第四次检测化学试卷(解析版) 题型:选择题
为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位学生分别设计了如下A~D四个实验,你认为结论不正确的是
A.将铜片放入稀硫酸中,无现象。若再向所得的溶液中加入硝酸银溶液,一段时间后,由于形成原电池,可看到有氢气产生
B.在相同条件下,等质量的大理石块和大理石粉与相同的盐酸反应,大理石粉反应快
C.将浓硝酸分别放在冷暗处和强光照射下,会发现光照可以加快浓硝酸的分解
D.两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省英文学校高一上学期12月月考化学试卷(解析版) 题型:选择题
下列反应的离子方程式正确的是
A.稀硫酸滴在银片上:2Ag+2H+===2Ag++H2↑
B.稀硫酸与氢氧化钡溶液混合:SO42-+Ba2+===BaSO4↓
C.稀硝酸滴在大理石上:CaCO3+2H+===Ca2++H2CO3
D.氧化铁与稀盐酸混合:Fe2O3+6H+===2Fe3++3H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com