
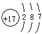
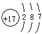
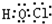
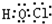
 ;由A、C、E三种元素组成的化合物具有漂白性,该化合物为HClO,分子中氧原子分别通过1对共用电子对与氢原子、氯原子连接,其电子式为
;由A、C、E三种元素组成的化合物具有漂白性,该化合物为HClO,分子中氧原子分别通过1对共用电子对与氢原子、氯原子连接,其电子式为 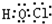 ,
, ;
;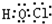 ;
;| 10-14 |
| 10-4 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
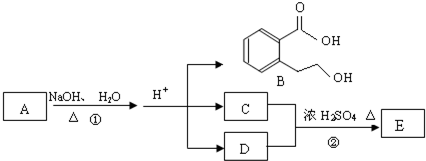
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |


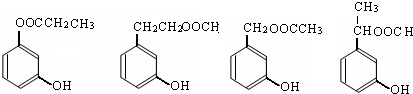

查看答案和解析>>
科目:高中化学 来源: 题型:
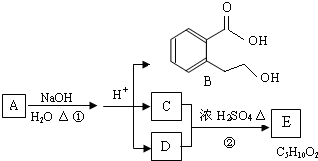
| 浓硫酸 |
| 加热 |
| 浓硫酸 |
| 加热 |


 写出四者之一即可
写出四者之一即可 写出四者之一即可
写出四者之一即可| 实验编号 | C物质的量浓度(mol?L-1) | NaOH物质的量浓度(mol?L-1) | 混合溶液的pH |
| m | 0.1 | 0.1 | pH=9 |
| n | 0.2 | 0.1 | pH<7 |
查看答案和解析>>
科目:高中化学 来源: 题型:







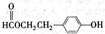
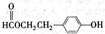
查看答案和解析>>
科目:高中化学 来源: 题型:

| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质编号 | 物质转化关系 | A | D | E |
| ① |  |
Si | SiO2 | H2SiO3 |
| ② | N2 | NO2 | HNO3 | |
| ③ | S | SO3 | H2SO4 | |
| ④ | Na | Na2O2 | NaOH |
| A、②③ | B、②④ |
| C、①③④ | D、①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com