
【题目】分现有部分元素的性质与原子(或分子)结构如下表:
元素编号 | 元素性质与原子(或分子)结构 |
X | 地壳中含量最高的非金属元素 |
Y | M层比K层多1个电子 |
Z | 最外层电子数为内层电子数的0.6倍 |
W | 与氯形成的氯化物是生活中常用的调味品 |
(1)X形成的双原子分子的结构式为 ,X形成的氢化物的沸点在同族元素形成的氢化物中是 (填“最高”或“最低”),原因是 。
(2)金属冶炼Y单质的化学方程式为 。
(3)Y单质与W元素的最高价氧化物对应水化物恰好反应完全,向反应后的溶液中通入过量的CO2,发生反应的离子方程式为 。
(4)单质Cu在一定条件下与足量Z元素形成的强酸浓溶液反应生成的气体是 (填化学式),检验该气体的常用试剂 。
【答案】(1)O =O,最高,水分子之间存在氢键
(2)2Al2O3![]() 4Al+3O2↑
4Al+3O2↑
(3)AlO2- + CO2 + 2H2O = Al(OH)3↓+ HCO3-
(4)SO2,品红溶液。
【解析】试题分析:X为地壳中含量最高的非金属元素,为O元素,Y的M层比K层多1个电子,为Al元素,Z的最外层电子数为内层电子数的0.6倍,为S元素,W与氯形成的氯化物是生活中常用的调味品,为Na元素。
(1)X为O,对应的双原子分子的结构式为O=O,对应的水中含有氢键,较一般的分子间作用力强,沸点较高,故答案为:O=O;最高;水分子间存在氢键;
(2)Y为Al,工业用电解熔融的氧化铝冶炼,方程式为2Al2O3![]() 4Al+3O2↑,故答案为:2Al2O3
4Al+3O2↑,故答案为:2Al2O3![]() 4Al+3O2↑;
4Al+3O2↑;
(3)Al单质与Na元素的最高价氧化物对应水化物恰好反应完全,生成NaAlO2,向反应后的溶液中通入过量的CO2,生成氢氧化铝和碳酸氢钠,发生反应的离子方程式为AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-,故答案为:AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-;
(4)单质Cu在一定条件下与足量Z元素形成的强酸浓溶液反应生成硫酸铜和二氧化硫气体,检验二氧化硫气体可用品红检验,如品红褪色,且加热溶液变红,故答案为:SO2;品红溶液。


科目:高中化学 来源: 题型:
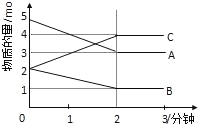
【题目】某可逆反应在某体积为5L的密闭容器中进行,在从0﹣3分钟各物质的量的变化情况如图所示(A、B、C均为气体).
(1)该反应的化学方程式为 ;
(2)反应开始至2分钟时,B的平均反应速率为 .
(3)能说明该反应已达到平衡状态的是 .
a.v(A)=2v(B)
b.容器内压强保持不变
c.v逆(A)=v正(C)
d.容器内混合气体的密度保持不变
(4)由如图求得A的平衡时的转化率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是制取干燥、纯净的氯气并验证氯气的性质的装置(加热及夹持装置省略)。

(1)写出装置A中制备氯气的化学反应方程式: 。
(2)装置C的作用是 。
(3)在反应过程中,装置D内干燥的蓝色石蕊试纸不变色,湿润的蓝色石蕊试纸先变红后退色,使试纸变红的物质是 (填化学式),使试纸退色的物质是 (填化学式)。
(4)装置D内湿润的KI淀粉试纸变蓝,说明Cl的非金属性 I的非金属性(填“大于”或“小于”)。
(5)该实验装置有个明显的缺陷是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于能量转换的认识中不正确的是
A.电解水生成氢气和氧气时,电能转化为化学能
B.白炽灯工作时,电能全部转化为光能
C.煤燃烧时,化学能主要转化为热能
D.绿色植物进行光合作用时,太阳能转化为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在硝酸铝和硝酸镁的混合溶液中,逐滴加入稀氢氧化钠溶液,直至过量.下列表示氢氧化钠加入量(x)与溶液中沉淀的量(y)的关系示意图中正确的是( )
A. B.
B. C.
C. D.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,充入SO2和18O原子组成的氧气,在一定条件下开始反应,在达到平衡后,18O存在于( )
A.只存在于氧气中 B.只存在于SO3中
C.只存在于SO2和SO3中 D.SO2、SO3、O2中都存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银铜合金广泛用于航空工业。从切割废料中回收并制备铜化工产品的工艺如下:

(注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃)
(1)电解精炼银时,阴极反应式为 ;滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,该气体变色的化学方程式为 。
(2)固体混合物B的组成为 ;在生成固体B的过程中,需控制NaOH的加入量,若NaOH过量,则因过量引起的反应的离子方程式为 。
(3)完成煅烧过程中一个反应的化学方程式: CuO+ Al2O3![]() CuAlO2+ ↑。
CuAlO2+ ↑。
(4)若银铜合金中铜的质量分数为63.5%,理论上5.0kg废料中的铜可完全转化为 molCuAlO2,至少需要1.0mol·L-1的Al2(SO4)3溶液 L。
(5)CuSO4溶液也可用于制备胆矾,其基本操作是 、过滤、洗涤和干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关.已知常温下,有下列3个装置.下列说法中正确的是( )

A.①②中Mg作负极,③中Fe作负极
B.②中Al作正极,其电极反应式为Al﹣3e﹣=Al3+
C.③中Fe作负极,电极反应式为Fe﹣2e﹣=Fe2+
D.若①②中转移的电子数相同,则①②中产生的H2的量也一定相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com