二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上可利用煤的气化产物(水煤气)合成二甲醚.
请回答下列问题:
(1)制水煤气的化学反应方程式为:
.
(2)利用水煤气合成二甲醚的三步反应如下:
①2H
2(g)+CO(g)?CH
3OH(g);△H=a kJ?mol
-1②2CH
3OH(g)?CH3OCH
3(g)+H
2O(g);△H=b kJ?mol
-1③CO(g)+H
2O(g)?CO
2(g)+H
2(g);△H=c kJ?mol
-1总反应:3H
2(g)+3CO(g)?CH
3OCH
3(g)+CO
2 (g)的△H=
;(与abc的函数关系).
若△H<0,一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是
(填字母代号).
a.高温 b.高压 c.减少CO
2的浓度
d.分离出二甲醚 e.增加CO的浓度 f.加入催化剂
(3)已知反应②2CH
3OH(g)?CH
3OCH
3(g)+H
2O(g).某温度下,在密闭容器中加入CH
3OH,反应到平衡时测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol?L-1) | 0.64 | 0.5 | 0.5 |
①比较此时正、逆反应速率的大小:v
正
v
逆 (填“>”、“<”或“=”).
②若加入CH
3OH后,经8min反应达到平衡,该时间内反应速率v(CH
3OH)=
.



 计算高手系列答案
计算高手系列答案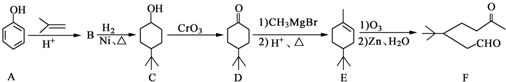
 )和CH2=CH2为原料制备有机物
)和CH2=CH2为原料制备有机物 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: