
| A. | 该反应中NH4NO3只作氧化剂 | |
| B. | ZnO是还原产物 | |
| C. | 氧化产物只有N2 | |
| D. | 该反应每生成1mol N2转移5mol电子 |
分析 NH4NO3+Zn=ZnO+N2↑+2H2O中,Zn元素的化合价升高,N元素的化合价由+5价降低为0,N元素的化合价由-3价升高为0,以此来解答.
解答 解:A.NH4NO3中N元素的化合价升高也降低,则既作氧化剂也作还原剂,故A错误;
B.Zn元素的化合价升高,失去电子被氧化,则ZnO为氧化产物,故B错误;
C.NH4NO3中-3价的N被氧化,Zn也被氧化,则氧化产物为ZnO和部分氮气,故C错误;
D.每生成1mol N2,1 moNH4lNO3转移电子由N元素的化合价升高可知,转移1mol×(5-0)=5mol电子,故D正确;
故选D.
点评 本题考查氧化还原反应,为高考常见题型,侧重氧化还原反应中基本概念的考查,把握元素的化合价变化即可解答,题目难度不大.


科目:高中化学 来源: 题型:解答题
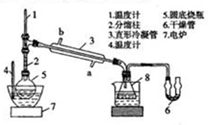 硼酸三甲酯可作溶剂、脱水剂和塑料、油漆、喷漆等的防火剂等.实验室合成硼酸三甲酯的反应、装置示意图及有关数据如下:
硼酸三甲酯可作溶剂、脱水剂和塑料、油漆、喷漆等的防火剂等.实验室合成硼酸三甲酯的反应、装置示意图及有关数据如下:| 硼酸三甲酯 | 甲醇 | |
| 相对分子量 | 104 | 32 |
| 溶解性 | 与乙醚、甲醇混溶,能水解 | 与水混溶 |
| 沸点/℃ | 68 | 64 |
| 备注 | 硼酸三甲酯与甲醇能形成共沸混合物,沸点54℃ | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
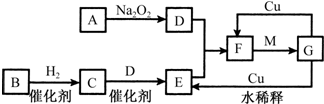
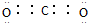 .
.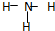 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数 C>B>D>A | B. | 单质熔点 D>B,A>C | ||
| C. | 原子半径 D>B>C>A | D. | 简单离子半径 C>A>D>B |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{94}^{238}$Pu与${\;}_{92}^{238}$U互为同位素 | |
| B. | ${\;}_{94}^{238}$Pu与${\;}_{94}^{239}$Pu互为同素异形体 | |
| C. | ${\;}_{94}^{238}$Pu与${\;}_{92}^{238}$U具有完全相同的化学性质 | |
| D. | ${\;}_{92}^{238}$Pu与${\;}_{92}^{239}$Pu具有相同的最外层电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
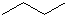
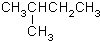
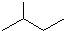 CH3CH=CHCH3
CH3CH=CHCH3
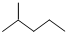 分子式C6H14用系统命名法对该有机物进行命名2-甲基戊烷
分子式C6H14用系统命名法对该有机物进行命名2-甲基戊烷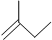 分子式C5H10③
分子式C5H10③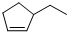 分子式C7H12
分子式C7H12查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Al3+、H+、AlO2-、Cl- | B. | Cu2+、Fe2+、ClO-、SO42- | ||
| C. | Na+、Ca2+、HCO3-、Cl- | D. | Cu2+、Fe3+、Cl-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com