
����Ŀ��ijǿ������ҺX�����ܺ���Al3+��Ba2+��NH4+��Fe2+��Fe3+��CO32-��SO42-��SiO32-��NO3-�е�һ�ֻ������ӣ�ȡ����Һ����ʵ�飬ת����ϵ��ͼ��ʾ����Ӧ��������һ�������ڿ����л��Ϊ����ɫ���ش��������⣺
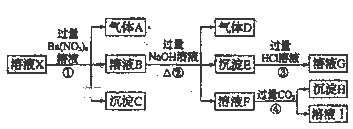
��1���������Ϣ��֪����ҺX��ȷ�������ڵ���������___��
��2������A��__(�ѧʽ)����������A�����ӷ���ʽΪ__��
��3��������з�����Ӧ�����ӷ���ʽΪ___��
��4�����������Ϣ��ͼ��ת����ϵ������ȷ����ҺX�п϶����ڵ�������__�����ܴ��ڵ�������__��������ܴ��ڵ������Ƿ���ڵķ�����__��
���𰸡�CO32-��SiO32-��NO3- NO 3Fe2++4H++NO3-=3Fe3++NO��+2H2O AlO2-+CO2+2H2O=Al(OH)3��+HCO3- Al3+��NH4+��SO42-��Fe2+ Fe3+ ȡ������ҺX���Թ��У��μӼ���KSCN��Һ������Һ���ɫ������ҺX�к���Fe3+������Һ�����ɫ������ҺX�в�����Fe3+
��������
��ǿ������Һ�У�CO32-��SiO32-���ܴ������ڣ�����Ba(NO3)2���ɳ���C������ҺX��һ������SO42-��X��һ��������Ba2+����������A���������ΪNO��ԭ��Һ��һ��������NO3-���������NaOH��Һ������������ΪNH3����X��һ������NH4+���������NaOH��Һ����������E���Ҵ˳����������ᣬ��X��һ������Fe2+�����ܺ���Fe3+����ҺF��ͨ�������CO2�����ɳ���H����X��һ������Al3+��
��1���������Ϣ�ķ�������ȷ����ҺX�в����ڵ������ӡ�
��2������A��NO����������NO��ԭ����Fe2+��������Һ����NO3-�����˷�Ӧ��
��3���������AlO2-�����CO2��ˮ��Һ�з�����Ӧ��
��4�����������Ϣ��ͼ��ת����ϵ������ȷ����ҺX�п϶����ڵ�����ΪAl3+��NH4+��SO42-��Fe2+�����ܴ��ڵ�������Fe3+��������ܴ��ڵ������Ƿ���ڣ���ʹ��KSCN��Һ��
��ǿ������Һ�У�CO32-��SiO32-���ܴ������ڣ�����Ba(NO3)2���ɳ���C������ҺX��һ������SO42-��X��һ��������Ba2+����������A���������ΪNO��ԭ��Һ��һ��������NO3-���������NaOH��Һ������������ΪNH3����X��һ������NH4+���������NaOH��Һ����������E���Ҵ˳����������ᣬ��X��һ������Fe2+�����ܺ���Fe3+����ҺF��ͨ�������CO2�����ɳ���H����X��һ������Al3+��
��1���������Ϣ�ķ�������ȷ����ҺX�в����ڵ�������ΪCO32-��SiO32-��NO3-����Ϊ��CO32-��SiO32-��NO3-��
��2������A��NO����������NO������Fe2+��������Һ����NO3-�����˷�Ӧ�����ӷ���ʽΪ3Fe2++4H++NO3-=3Fe3++NO��+2H2O����Ϊ��NO��3Fe2++4H++NO3-=3Fe3++NO��
+2H2O��
��3���������AlO2-�����CO2��ˮ��Һ�з�����Ӧ�����ӷ���ʽΪAlO2-+CO2+2H2O
=Al(OH)3��+HCO3-������AlO2-+CO2+2H2O=Al(OH)3��+HCO3-��
��4�����������Ϣ��ͼ��ת����ϵ������ȷ����ҺX�п϶����ڵ�����ΪAl3+��NH4+��SO42-��Fe2+�����ܴ��ڵ�������Fe3+��������ܴ��ڵ������Ƿ���ڵķ�����ȡ������ҺX���Թ��У��μӼ���KSCN��Һ������Һ���ɫ������ҺX�к���Fe3+������Һ�����ɫ������ҺX�в�����Fe3+����Ϊ��Al3+��NH4+��SO42-��Fe2+��Fe3+��ȡ������ҺX���Թ��У��μӼ���KSCN��Һ������Һ���ɫ������ҺX�к���Fe3+������Һ�����ɫ������ҺX�в�����Fe3+��


 ��������ϵ�д�
��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ű�����ཡ������������Ӱ�죮ȼú������β������ɿ�����Ⱦ��ԭ��֮һ��
��1������β����������Ҫԭ��Ϊ��2NO��g��+2CO![]() 2CO2��g��+N2��g����H��0
2CO2��g��+N2��g����H��0
�ٷ�Ӧ������-ʱ��ͼ����ͼ����ʾ���������������䣬���ڷ�Ӧǰ������ʵĴ�����������ʱ��ͼ����ͼ����ʾ������˵����ȷ����___________�����Ӧ��ĸ����
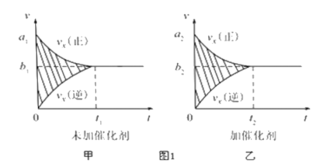
A�� a1��a2 B��b1��b2 C��t1��t2 D��ͼ������Ӱ�����������E��ͼ������Ӱ�����������
�����÷�Ӧ�ھ��ȡ����ݵ��ܱ���ϵ�н��У�����ʾ��ͼ��ȷ����˵����Ӧ�ڽ��е�t1ʱ�̴ﵽƽ��״̬����_________������ţ�

��2��ֱ���ŷ�úȼ�ղ������������������صĻ������⣮úȼ�ղ����������������������CH4����ԭNOx�������������������Ⱦ��
��֪��CH4��g��+2NO2��g��![]() N2��g��+CO2��g��+2H2O��g����H=��867kJ/mol
N2��g��+CO2��g��+2H2O��g����H=��867kJ/mol
2NO2��g��![]() N2O4��g����H=��56.9kJ/mol
N2O4��g����H=��56.9kJ/mol
H2O��g��=H2O��l����H=��44.0kJ/mol
д��CH4����ԭN2O4��g������N2��H2O��l�����Ȼ�ѧ����ʽ��______________��
��3��CH4��H2O��g���ڴ������淢����ӦCH4+H2OCO+3H2���÷�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ�������
�¶�/�� | 800 | 1000 | 1200 | 1400 |
ƽ�ⳣ�� | 0.45 | 1.92 | 276.5 | 1771.5 |
�ٸ÷�Ӧ��_________��Ӧ��������������������������
��T��ʱ����1L�ܱ�������Ͷ��lmolCH4��lmolH2O��g����ƽ��ʱc��CH4��=0.5mol/L�����¶��·�ӦCH4+H2O![]() CO+3H2��ƽ�ⳣ��K=______________��
CO+3H2��ƽ�ⳣ��K=______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����3mol/L NaOH��Һ���뵽25mL һ��Ũ�ȵ�AlCl3��Һ�С���ͼ���������̵���ѧ�������ߡ����к����ʾ����OH-�����ʵ����������ʾ������Al(OH)3���������ʵ������ͼ�ش�
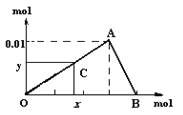
��1����C���O����A���˶�ʱ����ʾ��OH-�IJ��ϼ��룬��������________��OA���߱�ʾ�����ӷ�Ӧ��________________���ɴ˿ɵ�A�������Ϊ_______��
��2����C���A����B���˶�ʱ����ʾ��_____��AB���߱�ʾ�����ӷ�ӦΪ��______���ɴ˿ɵ�B�������Ϊ��__________��
��3�������������������AlCl3��Һ��Al3+���ӵ�Ũ��Ϊ��_____mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ϊ��Ҫ�ĺ�������γ��������Ҫ��Ⱦ��֮һ��
��1����ʵ�����У�����70����������Һ���������Ʒ�ĩ��Ӧ��ȡ��������Ҫ����Ʒ�Ӧ���ʣ���ѡ����ͼ��ʾ���巢��װ���е�_____(�����������ĸ)��
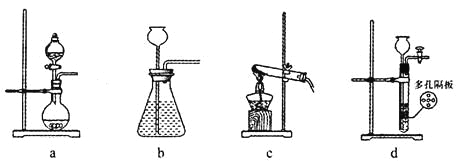
��2��SO2��������������SO3���÷�Ӧ���Ȼ�ѧ����ʽΪ��2SO2(g)+O2(g)![]() 2SO3(g) ��H="a" kJ��mol-1����T1��ʱ����2 mol SO2��1mol O2�����ݻ�Ϊ2 L���ܱ�����A�У���ַ�Ӧ���ﵽƽ�⣬�˹����зų�����98��3 kJ�����SO2��ƽ��ת����Ϊ50������a=_____��T1��ʱ��������Ӧ��ƽ�ⳣ��K1=____L��mol-1��������ʼ�¶�ΪT1����2 mol SO2��1 molO2�����ݻ�Ϊ2 L�ľ����ܱ�����B�У���ַ�Ӧ����T2��ʱ�ﵽƽ�⣬�ڴ��¶�ʱ������Ӧ��ƽ�ⳣ��ΪK2����K1______K2(����>������<������=��)��
2SO3(g) ��H="a" kJ��mol-1����T1��ʱ����2 mol SO2��1mol O2�����ݻ�Ϊ2 L���ܱ�����A�У���ַ�Ӧ���ﵽƽ�⣬�˹����зų�����98��3 kJ�����SO2��ƽ��ת����Ϊ50������a=_____��T1��ʱ��������Ӧ��ƽ�ⳣ��K1=____L��mol-1��������ʼ�¶�ΪT1����2 mol SO2��1 molO2�����ݻ�Ϊ2 L�ľ����ܱ�����B�У���ַ�Ӧ����T2��ʱ�ﵽƽ�⣬�ڴ��¶�ʱ������Ӧ��ƽ�ⳣ��ΪK2����K1______K2(����>������<������=��)��
��3��ij�ȵ糧�Ͽմ��������������������س��꣬�ֶԸ�������ˮ��Ʒ����̽����������pH��ֽ�ⶨ��ˮ��Ʒ��pH����������Ϊ___________________________�������ƷpHԼΪ3��Ϊ��һ��̽����SO3���γ���������ʣ���һ������SO2ͨ������ˮ�У����pHΪ3����Һ��Ȼ����Һ��ΪA��B���ݣ���A�м���������NaOH���壬ʹ��Һǡ�ó�����(���������������ʺ������������ʵ�Ӱ��)�����������Һ�����ӵ�Ũ�ȼ���ڵĹ�ϵʽΪ��[Na+]=______________������ҺB�����ڿ����У������ǰ��ȣ����ú����ҺB��ˮ�ĵ���̶Ƚ�__________(����������������С������������)��
��4����ҵ�ϳ�������ͼ��ʾ�����̴�����ҵβ���е�SO2��
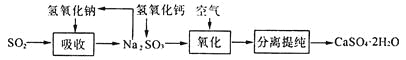
������������һ�����ʿ�������ѭ�����ã������������Ļ�ѧ����ʽΪ_______________.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��500 mL KNO3��Cu(NO3��2�Ļ����Һ��c(NO![]() ����0.6 mol��L��1����ʯī���缫������Һ����ͨ��һ��ʱ����������ռ���2.24 L����(��״���£����ٶ�������Һ�����Ϊ500 mL������˵����ȷ����
����0.6 mol��L��1����ʯī���缫������Һ����ͨ��һ��ʱ����������ռ���2.24 L����(��״���£����ٶ�������Һ�����Ϊ500 mL������˵����ȷ����
A.ԭ�����Һ��c(K����Ϊ0.2 mol��L��1
B.�����������й�ת��0.2 mol����
C.���õ���Cu�����ʵ���Ϊ0.05 mol
D.������Һ��c(H����Ϊ0.2 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ƭ��ϩ�������һ��̫���ܴ��ܲ��ϡ�����Ƭ��ϩ�������������¿��Է�������ת��������˵��������ǣ� ��
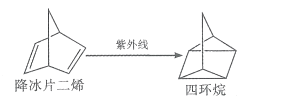
A. ����Ƭ��ϩ���Ļ��黥Ϊͬ���칹��
B. ����Ƭ��ϩ��ʹ���Ը��������Һ��ɫ
C. �Ļ����һ�ȴ��ﳬ�����֣������������칹��
D. ����Ƭ��ϩ������λ��ͬһƽ���̼ԭ�Ӳ�����4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҵ�����Ҫ�Ļ���ԭ�ϣ�Ҳ��������Դ��
��ҵ�ϣ���һ������������ϩˮ�����Ʊ��Ҵ�����֪�Ȼ�ѧ����ʽ���£�
��CH2=CH2(g)+H2O(g)CH3CH2OH(g) ��H1
��2CH2=CH2(g)+H2O(g)CH3CH2OCH2CH3(g) ��H2
��2CH3CH2OH(g)CH3CH2OCH2CH3(g)+H2O(g) ��H3
��1�����ֻ�ѧ���ļ������£�
��ѧ�� | H-C | C=C | H-O | C-O | C-C |
����kJ��mol-1 | 413 | 615 | 463 | 351 | 348 |
���ݼ��ܼ��㦤H1=________________kJ��mol-1��
��2���ں����ܱ������з�����Ӧ�ڣ�������˵���÷�Ӧ�ﵽƽ�����_________��
a����������ѹǿ���ֲ���
b��H2O(g)������������CH3CH2OCH2CH3(g)�����������
c������ƽ��Ħ���������ֲ���
d�������������ܶȱ��ֲ���
��3�����ܱ�������Ͷ��CH2=CH2(g)��H2O(g)�ʹ���������Ӧ�٣���ϩ��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��

��x����________________����ѡ��¶ȡ���ѹǿ����
��L1��L2�ĸ�����˵�����ɣ�_____________________________________________________��
����ͼ��ʾ���ס���֮��ĸ���K�ͻ���F���������ƶ������г���2molA��1molB�����г���2molC��lmolHe����ʱKͣ��0������һ�������·������淴Ӧ��2A(g)+B(g)2C(g)����Ӧ�ﵽƽ����ٻָ���ԭ�¶ȡ��ش��������⣺

��4���ﵽƽ��ʱ������K����ͣ����0�̶����ijһ������Ϊa������a��ȡֵ��Χ��__________��
��5�����ﵽƽ��ʱ������K����ͣ�������̶�1������ʱ���ݻ�Ϊ2L����÷�Ӧ��ѧƽ�ⳣ��Ϊ_______________��
��6����һ��ʼ�ͽ�K��F����ͼ�̶����������������䣬��ﵽƽ��ʱ����ü���A��ת����Ϊb��������C��ת����Ϊ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪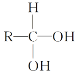
![]() R��CHO������A��B��C��D��E��F�����л���������ת����ϵ������A�ķ���ʽΪC4H8O3�������ж���ȷ����(����)
R��CHO������A��B��C��D��E��F�����л���������ת����ϵ������A�ķ���ʽΪC4H8O3�������ж���ȷ����(����)
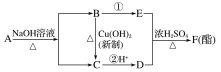
A.�л���A�ṹ����������
B.��Ӧ������������Ӧ
C.�л���B��D�����ʽ��ͬ
D.�л���E�ǽ������Ƽݵ���Ҫ��֤
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�����ȿ���CO��CO2��Ӧ�öԹ�����̬������������Ҫ�����塣
(1)��֪7gCO��ȫȼ�շ���70.7kJ��д��COȼ�շ�Ӧ���Ȼ�ѧ����ʽ_________��
(2)CO��O2��Ƴ�ȼ�ϵ�أ���KOH��ҺΪ���Һ�����õ�صĸ�����ӦʽΪ_______���øõ�ص�⾫��ͭ����ͭ��ͨ��______һ��������CO������O2����������
(3)���ù��ܺ�������ɽ�CO2��H2O(g)ת��ΪCH4��O2�����������ʱ���ڲ�ͬ������I��II��III�������£�CH4���������ʱ��ı仯����ͼ����0��15Сʱ�ڣ�CH4��ƽ����������I��II��III��С�����˳��Ϊ___________������ţ���

(4)��TiO2��Cu2Al2O4Ϊ���������Խ�CO2��CH4ֱ��ת�������ᡣ�ڲ�ͬ�¶��´����Ĵ�Ч����������������ʵĹ�ϵ����ͼ��
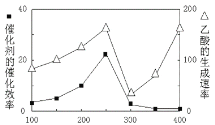
�ٵ��¶���________��Χʱ���¶��������������ʵ���ҪӰ�����ء�
��Cu2Al2O4������ϡ���ᣬϡ���ỹԭ����ΪNO��ͬʱ���������Σ�д���йص����ӷ���ʽ___________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com