
美国《探索》杂志报道:科学家对加拿大安大略湖北部的湖泊进行了研究,科学家们最终证实使死区“起死回生”的关键性因素是控制湖泊流域中的磷含量。综合上述信息,下列说法正确的是( )
①赤潮与水华都与氮、磷的富营养化有关 ②海藻降解时会消耗水体中的氧气,导致水体缺氧,水生动物死亡 ③早期使用的洗衣粉中添加的“Na5P3O10”,能除去自来水中的Ca2+和Mg2+等 ④有科学家提出在南极播种铁质,促进藻类大量繁殖,其研究目的可能是扼制温室气体的增加
A.①②③④ B.①④
C.②③ D.①②③
 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
实验室制取SO2的反应原理为Na2SO3+H2SO4(浓)===Na2SO4+SO2↑+H2O。请用下列装置设计一个实验,以测定SO2转化为SO3的转化率:
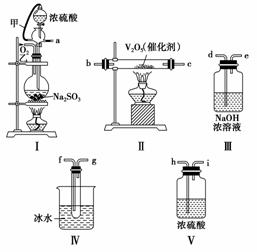
(1)这些装置的连接顺序(按气体从左到右的方向)是________→________→________→________→________→________→________→________(填各接口的编号)。
(2)实验时甲橡皮管的作用与原理是__________________________________________________________
__________________________________________________________。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是__________________________________________________________
__________________________________________________________。
(4)Ⅳ处观察到的现象是__________________________________________________________。
(5)在Ⅰ处用大火加热烧瓶时,SO2的转化率会________(填“增大”、“不变”或“减小”)。
(6)用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重m g,则本实验中SO2的转化率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,下列溶液的离子浓度关系式正确的是( )
A.pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5 mol·L-1
B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH-)+c(HC2O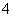 )
)
D.pH相同的①CH3COONa,②NaHCO3,③NaClO三种溶液的c(Na+):①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
滴定分析是一种操作简便、准确度很高的定量分析方法,它可广泛应用于中和滴定、氧化还原反应等滴定中。某研究性学习小组的同学利用滴定分析法进行下面两项定量分析。
(1)测定NaOH和Na2CO3的混合液中NaOH的含量。实验操作为先向混合液中加过量的BaCl2溶液使Na2CO3完全转化成BaCO3沉淀,然后用标准盐酸滴定(用酚酞作指示剂)。
①向混有BaCO3沉淀的NaOH溶液中直接滴入盐酸,则终点颜色的变化为______________,为何此种情况能测出NaOH的含量?________________。
②滴定时,若滴定管中的滴定液一直下降到活塞处才达到滴定终点,则能否由此准确地计算出结果?________________________________________________________________________,
请说明理由:__________________________________________________________________。
(2)测定某品牌的碘盐(含有碘酸钾)中碘元素的百分含量。准确称取5.000 0 g该碘盐,溶于蒸馏水,然后与足量的KI溶液在酸性条件下混合(发生的反应为KIO3+3H2SO4+5KI===3K2SO4+3I2+3H2O),充分反应后将混合

溶液稀释至250 mL,然后用5.0×10-4 mol·L-1的Na2S2O3标准溶液进行滴定(用淀粉作指示剂,反应为I2+2S2O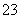 ===2I-+S4O
===2I-+S4O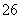 )。取用Na2S2O3的标准溶液应该用________式滴定管。有关实验数值如下表所示(第一次滴定终点的数据如图所示,请将读得的数据填入表中)。
)。取用Na2S2O3的标准溶液应该用________式滴定管。有关实验数值如下表所示(第一次滴定终点的数据如图所示,请将读得的数据填入表中)。
| 滴定次数 | 待测液的 体积(mL) | 滴定前的 读数(mL) | 滴定后的 读数(mL) |
| 第一次 | 25.00 | 0.00 | V=________ |
| 第二次 | 25.00 | 0.00 | 14.99 |
| 第三次 | 25.00 | 0.00 | 15.01 |
该碘盐中碘元素的百分含量为________,下列操作中,会导致所测得的碘元素的百分含量偏大的是________。
a.滴定终点时,俯视刻度
b.没有用Na2S2O3标准溶液润洗相应的滴定管
c.锥形瓶中有少量的蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与社会、生产、生活密切相关。下列说法正确的是( )
A.石英只能用于生产光导纤维
B.从海水中提取物质都必须通过化学反应才能实现
C.为了增加食物的营养成分,可以大量使用食品添加剂
D.“地沟油”禁止食用,但可以用来制肥皂
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温下,0.1 mol·L-1某一元酸HA在水中有0.1%发生电离。下列叙述正确的是( )
A.该溶液的pH=3
B.升高温度,溶液的pH增大
C.此酸的电离平衡常数约为1×10-7
D.由HA电离出的c(H+)约为水电离出的c(H+)的105倍
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,现有0.1 mol·L-1的氨水。请回答下列问题:
(1)为了证明一水合氨(NH3·H2O)是弱电解质,常温下,甲、乙、丙三人分别选用下列试剂进行实验:0.010 mol·L-1氨水、0.1 mol·L-1 NH4Cl溶液,NH4Cl晶体、酚酞试剂、pH试纸、蒸馏水。
①甲用pH试纸测出0.010 mol·L-1氨水的pH为10,则认定一水合氨是弱电解质,你认为这一方法是否正确?________(填“是”或“否”),请说明理由:__________________________________________________________
__________________________________________________________。
②乙取出10 mL 0.010 mol·L-1氨水,用pH试纸测出其pH=a,然后用蒸馏水稀释至1 000 mL,再用pH试纸测出pH为b,若要确认NH3·H2O是弱电解质,则a、b应满足关系:________________(用等式或不等式表示)。
③丙取出10 mL 0.010 mol·L-1氨水,滴入2滴酚酞试剂,显粉红色,再加入少量NH4Cl晶体,颜色变________(填“深”或“浅”)。你认为这一方法能否证明NH3·H2O是弱电解质?________(填“能”或“否”),并说明原因:__________________________________________________________
__________________________________________________________。
(2)若向氨水中加入少量硫酸铵固体,此时溶液中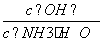 ________(填“增大”、“减小”或“不变”)。
________(填“增大”、“减小”或“不变”)。
(3)若向氨水中加入稀硫酸,二者恰好完全反应后所得溶液的pH________7(填“>”、“<”或“=”),用离子方程式解释原因:__________________________________________________________
__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
①溶液、②胶体、③悬浊液、④乳浊液是四种常见的分散系,静置,分散质和分散剂很快分离,其中产生沉淀的是__________;分散系分层的是____________;用一束平行光照射,出现一条明亮“光路”的是________;能通过半透膜的是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com