



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �����£���1.00mol/L�������20.00mL 1.00mol/L��ˮ�У���ҺpH���¶ȣ��棩
�����£���1.00mol/L�������20.00mL 1.00mol/L��ˮ�У���ҺpH���¶ȣ��棩+ 4 |
| ����Ũ�ȵĹ�ϵ | ���� | ��Һ��pH | �����غ��ϵ | |
| �� | C��NH4+����C��Cl-����C��OH-����C��H+�� | NH4Cl��NH3?H2O NH4Cl��NH3?H2O |
pH��7 | / |
| �� | NH4Cl | / | c��NH4+��+c��NH3?H2O��=c��Cl-�� c��NH4+��+c��NH3?H2O��=c��Cl-�� | |
| �� | C��Cl-����C��H+����C��NH4+����C��OH-�� | NH4Cl��HCl NH4Cl��HCl |
pH��7 | / |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| T/K | 303 | 313 | 323 | 353 |
| NH3������/��10-6 mol�� | 4.8 | 5.9 | 6.0 | 2.0 |
| 3 |
| 2 |
| 4 |
| 7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
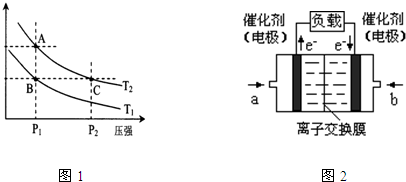
�������糧�ͷų������ĵ������NOx������������Ͷ�����̼���������ɻ�����Ⱦ����ȼú���������������������̼�ȴ�������ʵ����ɫ���������ܼ��š��������õ�Ŀ�ġ�
��1�����������ü������ԭNOx��
CH4��g����4NO2��g����4NO��g����CO2��g����2H2O��g����H1��-574 kJ��mol��1
CH4��g����4NO��g����2N2��g����CO2��g����2H2O��g����H2��-1160 kJ��mol��1
����ֱ�ӽ�NO2��ԭΪN2���Ȼ�ѧ����ʽΪ__________��
��2����̼����CO2ת��Ϊ�״����Ȼ�ѧ����ʽΪ��
CO2��g����3H2��g��![]() CH3OH��g����H2O��g�� ��H3
CH3OH��g����H2O��g�� ��H3
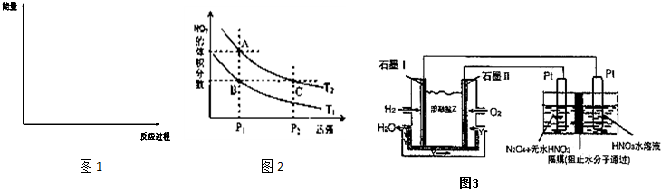
��ȡ��ݵ����CO2��H2�Ļ�����壨���ʵ���֮�Ⱦ�Ϊ1��3�����ֱ�����¶Ȳ�ͬ���ݻ���ͬ�ĺ����ܱ������У�����������Ӧ����Ӧ��ͬʱ���ü״�����������գ�CH3OH�� �뷴Ӧ�¶�T�Ĺ�ϵ��������ͼ��ʾ��������CO2ת��Ϊ�״��ķ�Ӧ�ġ�H3__________0�����������������������

����һ���º����ܱ������г���1 mol CO2��3 mol H2������������Ӧ�����CO2��CH3OH��g����Ũ����ʱ��仯������ͼ��ʾ������˵����ȷ����__________������ĸ���ţ���

A����10 min������������ٳ���1 mol CO2��3 mol H2�����ٴδﵽƽ��ʱc��CH3OH��=1��5 mol/L
B��0~10 min�ڣ�������ƽ����Ӧ����[Ϊ0��075 mol/��L��min��
C���ﵽƽ��ʱ��������ת����Ϊ0��75
D�����¶��£���Ӧ��ƽ�ⳣ����ֵΪ3/16
E�������¶Ƚ�ʹn��CH3OH��/n��CO2����С
��ֱ�Ӽ״�ȼ�ϵ�ؽṹ������ͼ��ʾ���乤��ʱ�����ĵ缫��Ӧʽ�ɱ�
ʾΪ ��

��3������ij���������н���������������һ�����İ�����������Ӧ����������狀�����淋Ļ������Ϊ����Ʒ���ʡ�����狀�����淋�ˮ��Һ��pH��7������ԭ�����һ�����ӷ���ʽ��ʾΪ�� ����һ�����ʵ���Ũ�ȵ��������Һ�еμ�������NaOH��Һ��ʹ��Һ��pH=7������Һ��c��Na+��+c��H+��__________c��NO3-��+c��OH-������д������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ͬ���� ���ͣ������


�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com