
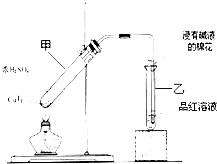
 某教师在课堂上用右图所示的装置来验证浓硫酸与铜是否发生反应,并探讨反应所产生气体的性质.请回答下列问题:
某教师在课堂上用右图所示的装置来验证浓硫酸与铜是否发生反应,并探讨反应所产生气体的性质.请回答下列问题: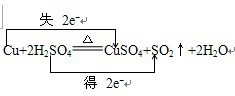 .
.分析 (1)金属铜和浓硫酸发生反应生成硫酸铜、水和二氧化硫,二氧化硫能使品红褪色,具有漂白性;
(2)金属铜和浓硫酸发生反应生成硫酸铜、水和二氧化硫,根据化合价的升高值=化合价的降低值=转移电子数来标电子转移情况;
(3)二氧化硫有毒,属于酸性氧化物,能和碱反应;
(4)①写出反应的化学方程式,根据氢氧化钡的物质的量计算出二氧化硫的物质的量,再计算出标况下二氧化硫的体积;
②利用极值法讨论沉淀的组成成分.
解答 解:(1)金属铜和浓硫酸发生反应生成硫酸铜、水和二氧化硫,生成的二氧化硫能使品红褪色,说明二氧化硫具有漂白性,
故答案为:品红溶液褪色;漂白;
(2)金属铜和浓硫酸发生反应生成硫酸铜、水和二氧化硫:Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O,化合价的升高值=化合价的降低值=转移电子数=2,用单线桥表示电子转移情况如下: ,故答案为:
,故答案为: ;
;
(3)二氧化硫有毒,属于酸性氧化物,能和碱反应生成盐和水,在装置口处浸有碱液的棉花可以和二氧化硫反应,
故答案为:吸收SO2;
(4)①二氧化硫和氢氧化钡的反应方程式为:SO2+Ba(OH)2=BaSO3↓+H2O,
20.00mL 0.5mol/L的 Ba(OH)2溶液中含有氢氧化钡的物质的量为:0.5mol/L×0.02L=0.01mol,根据反应可知,空气中含有二氧化硫的物质的量与氢氧化钡的物质的量相等,都是0.01mol,标况下0.01mol二氧化硫的体积为:22.4L/mol×0.01mol=0.0224L=22.4mL,
答:该雨水中共溶解标准状况下SO2的体积为22.4mL;
②0.5mol/L 20.00mL 的Ba(OH)2溶液和二氧化硫反应,如果全部转化为亚硫酸钡,根据钡原子守恒,则生成亚硫酸钡的质量为:0.01mol×217g/mol=2.17,如果全部转化为硫酸钡,根据钡原子守恒,则生成硫酸钡的质量为:0.01mol×233g/mol=2.33g,2.17g<2.250g<2.33g,
所以沉淀物的组成为BaSO3和BaSO4,
答:生成的沉淀为BaSO3和BaSO4的混合物.
点评 本题考查了浓硫酸的性质、化学方程式的计算、氧化还原反应的应用等知识,题目难度中等,注意掌握氧化还原反应的实质、浓硫酸的性质,明确极值法在化学计算中的应用方法.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 甲醛 | B. | 乙醇 | C. | 甲烷 | D. | 二氧化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水由液态变为玻璃态,体积缩小 | |
| B. | 水由液态变为玻璃态,体积膨胀 | |
| C. | 玻璃态是水的一种特殊状态晶体 | |
| D. | 玻璃态水是水分子在空间有规则排列形成的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
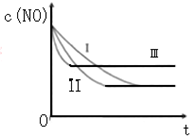 汽车尾气中的主要污染物是NO和CO.为了减轻大气污染,人们提出通过以下反应来处理汽车尾气:
汽车尾气中的主要污染物是NO和CO.为了减轻大气污染,人们提出通过以下反应来处理汽车尾气:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| C(NO)10-4 mol/L | 10.0 | 4.50 | C1 | 1.50 | 1.00 | 1.00 |
| C(CO)10-3 mol/L | 3.60 | 3.05 | C2 | 2.75 | 2.70 | 2.70 |
| 实验 编号 | T/°C | NO初始浓 度/10-3mol•L-1 | CO初始浓 度/10-3mol•L-1 | 催化剂的比 表面积/m2•g-1 |
| ① | 350 | 1.20 | 5.80 | 124 |
| ② | 280 | 1.20 | 5.80 | 124 |
| ③ | 280 | 1.20 | 5.80 | 82 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
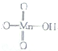 它属于强(填“强”或“弱”)酸.
它属于强(填“强”或“弱”)酸.| 化学键 | H-O | O-O | O-O |
| 键能/(J.mol-1) | 163 | 142 | 438 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com