
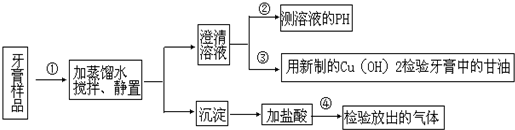
分析 (1)A.分离溶液和不溶物的方法为过滤;
B.溶液中含有氟化钠,氟离子部分水解生成氟化氢和氢氧根离子;
C.甘油和氢氧化铜之间反应生成的不是沉淀;
D.二氧化碳请通知含有氯化氢气体或二氧化碳过量在石灰水中生成碳酸氢钙,则溶液不会变浑浊;
(2)草酸根离子与钙离子反应生成草酸钙沉淀.
解答 解:(1)A.将固体和溶液分离的方法是过滤,可通过倾析法分离溶液和沉淀,故A正确;
B.溶液中氟离子水解溶液呈碱性,则在②中,测得pH>7,可能是牙膏成分中NaF水解引起的,故B正确;
C.甘油和新制氢氧化铜之间的反应为: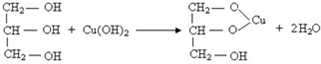 ,所得的溶液显示绛蓝色,据此可检验甘油,但是生成的不是沉淀,故C错误;
,所得的溶液显示绛蓝色,据此可检验甘油,但是生成的不是沉淀,故C错误;
D.如果生成的二氧化碳气体中含有氯化氢气体,或二氧化碳量多在氢氧化钙溶液中生成碳酸氢钙溶液,则在④中放出的气体通过澄清石灰水不一定出现沉淀,故D正确;
故答案为:C;
(2)草酸根离子与钙离子反应生成草酸钙沉淀,所以检验钙离子,可以用草酸铵溶液,
故答案为:草酸铵溶液.
点评 本题考查了探究物质组成的方法,题目难度中等,明确探究原理及常见物质的性质及检验方法为解答关键,试题侧重考查学生的分析、理解能力及化学实验能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | ||
| Y | ||
| Z |
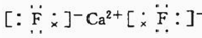 ,属于离子晶体.
,属于离子晶体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子晶体中相对分子质量大的熔、沸点一定比相对分子质量小的高 | |
| B. | 在氯化钠晶体中,每个氯离子周围都紧邻12个氯离子 | |
| C. | 在金属铜的晶体中,由于存在自由电子,因此铜能导电 | |
| D. | 金刚石的网状结构中,最小的环上有6个碳原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{5}$mol | B. | $\frac{2}{5}$ mol | C. | $\frac{3}{5}$mol | D. | $\frac{11}{5}$ mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用移液管移取10 mL NaOH溶液放于锥形瓶中,移液管的尖嘴和锥形瓶内壁一定要接触 | |
| B. | 实验室制硝基苯时,先将硝酸与浓硫酸混合,冷却后边振荡边滴加苯 | |
| C. | 制备硝酸钾晶体实验中先后进行了二次过滤,分别是先常温减压过滤、后高温常压过滤 | |
| D. | 受溴腐蚀致伤:先用苯或甘油洗伤口,再用水洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油裂解、煤的气化、海水制镁都包含化学变化 | |
| B. | 福尔马林用于制备标本是利用了其使蛋白质变性的性质 | |
| C. | 红葡萄酒储藏时间长后变香可能是因为乙醇发生了酯化反应 | |
| D. | 做衣服的棉和麻均与淀粉互为同分异构体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com