
化学与生产、生活密切相关,下列说法正确的是
A.焰火的五彩缤纷是某些金属元素化学性质的展现
B.将煤气化后再作为能源,可减少PM2.5引起的危害
C.用激光笔分到照射盛有蓝墨水、FeCl3 溶液的玻璃杯均出现光亮的通路
D.氨气液化时能吸收大量的热,常用来做冷冻剂
科目:高中化学 来源:2014-2015浙江省台州市高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列物质中既能发生加成也能发生取代反应且同时能使溴水因反应褪色,也能使高锰酸钾酸性溶液褪色的是
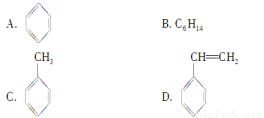
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省邛崃市高一下学期第一次月考化学试卷(解析版) 题型:选择题
现代生活中,人们出行的代步工具多种多样,消耗的能量类型各不相同。自行车、电动自行车、普通汽车消耗的能量类型分别是①生物质能②核能③电能④太阳能⑤化学能
A.①④⑤ B.①③⑤ C.①②③ D.①③④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省八市高三教学质量监测考试理科综合化学试卷(解析版) 题型:填空题
选考【化学——选修5,有机化学基础】(15分)高聚酚酯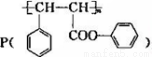 是一种环保型的新涂料,其合成路线如下图所示:’
是一种环保型的新涂料,其合成路线如下图所示:’

请回答下列问题:
(1)P的分子式为________,反应①属于________反应,反应①还有多种有机副产物,其中能使溴的CCl4溶液褪色的副产物的结构筒式为________。
(2)若反应②中两种反应物物质的量之比为1:1,则除A外另一种产物的名称是________,E是高分子化台物,其结构筒式为________。
(3)C转化为D的化学方程式是______________________.
(4)B有多种同分异构体,符舍下列条件的同分异构体共有_____种,其中校磁共振氢谱中有6组峰的是_________(写出其中一种的结构简式)。
①能与NaHCO3 溶液反应
②遇3溶液显紫色
③分子中含一个-CH3
(5)由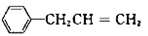 合成B的另一种途径为
合成B的另一种途径为

则F中官能团名称是_________,H的结构简式为_________,试剂G的化学式_________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省八市高三教学质量监测考试理科综合化学试卷(解析版) 题型:选择题
某强酸性溶液中可能存在 中的若干种,现取适量溶液进行如下实验
中的若干种,现取适量溶液进行如下实验

下列有关判断正确的是
A.原溶液中一定有.
B.原溶液中一定没有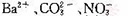
c.步骤③中反应的离子方程式为
D.气体A、B之间肯定不能发生反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省惠州市高三4月模拟考试理综化学试卷(解析版) 题型:选择题
物质中杂质(括号内为杂质)的检验、除杂的试剂或方法都正确的是
物质及其杂质 | 检验 | 除杂 | |
A | Cl2(HCl) | 湿润的淀粉KI试纸 | 饱和食盐水 |
B | NO(NO2) | 观察颜色或湿润的淀粉KI试纸 | 水 |
C | CO2(HCl) | AgNO3溶液(含稀硝酸) | 饱和NaHCO3溶液 |
D | NaHCO3溶液(Na2CO3) | Ca(OH)2溶液 | 过量CO2 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省惠州市高三4月模拟考试理综化学试卷(解析版) 题型:选择题
下列有关说法中,正确的是
A.糖类、油脂和蛋白质都是天然高分子化合物
B.用福尔马林(甲醛溶液)浸泡海产品,可长时间保鲜
C.粮食酿酒主要经过淀粉→葡萄糖→乙醇的化学变化过程
D.明矾既可用于净水,也可杀菌消毒
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三第二次模拟考试化学试卷(解析版) 题型:填空题
(12分)碱式次氯酸镁[Mga(ClO)b(OH)c·xH2O]是一种有开发价值的微溶于水的无机抗菌剂。为确定碱式次氯酸镁的组成,进行如下实验:
①准确称取1.685 g碱式次氯酸镁试样于250 mL锥形瓶中,加入过量的KI溶液,用足量乙酸酸化,用0.800 0 mol·L-1的Na2S2O3标准溶液滴定至终点(离子方程式为2S2O32-+I2===2I-+S4O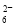 ),消耗25.00 mL。
),消耗25.00 mL。
②另取1.685 g碱式次氯酸镁试样,用足量乙酸酸化,再用足量3%H2O2溶液处理至不再产生气泡(H2O2被ClO-氧化为O2),稀释至1 000 mL。移取25.00 mL溶液至锥形瓶中,在一定条件下用0.020 00 mol·L-1的EDTA(Na2H2Y)标准溶液滴定其中的Mg2+(离子方程式为Mg2++H2Y2-===MgY2-+2H+),消耗25.00 mL。
(1)步骤①需要用到的指示剂是________。
(2)步骤②若滴定管在使用前未用EDTA标准溶液润洗,测得的Mg2+物质的量将________(填“偏高”“偏低”或“不变”)。
(3)通过计算确定碱式次氯酸镁的化学式(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省常德市高三模拟考试理综化学试卷(解析版) 题型:填空题
目前半导体生产展开了一场“铜芯片”革命——在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:

回答下列问题:
(1)基态铜原子的电子排布式为 ,硫、氧元素相比,第一电离能较小的元素是 (填元素符号)。
(2)反应①、②中均生成有相同的气体分子,该分子的中心原子杂化类型是 ,其立体结构是 。
(3)某学生用硫酸铜溶液与氨水做了一组实验:CuSO4溶液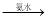 蓝色沉淀
蓝色沉淀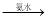 沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式 ;深蓝色透明溶液中的阳离子(不考虑H+)内存在的全部化学键类型有 。
沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式 ;深蓝色透明溶液中的阳离子(不考虑H+)内存在的全部化学键类型有 。
(4)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途,铜晶体中铜原子堆积模型为 ;铜的某种氧化物晶胞结构如图所示,若该晶体的密度为d g/cm3,阿伏加德罗常数的值为NA,则该晶胞中铜原子与氧原子之间的距离为 pm。(用含d和NA的式子表示)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com