
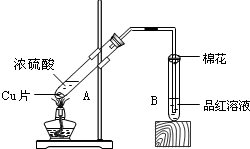
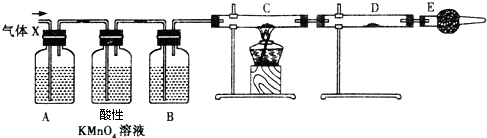
 某校化学组的同学用如图装置对铜与浓硫酸在一定条件下的反应进行实验探究,请回答:
某校化学组的同学用如图装置对铜与浓硫酸在一定条件下的反应进行实验探究,请回答:分析 I.加热条件下,浓硫酸和Cu发生氧化还原反应生成硫酸铜、二氧化硫和水;Cu与浓硫酸反应与稀硫酸不反应;
II.生成的二氧化硫有毒,是大气污染物,所以要进行处理,利二氧化硫为酸性还原性气体.
解答 解:I.加热条件下,浓硫酸和Cu发生氧化还原反应生成硫酸铜、二氧化硫和水,反应方程式为Cu+2H2SO4 (浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;Cu与浓硫酸反应与稀硫酸不反应,1mol Cu与2mol浓硫酸充分反应硫酸不能全部反应,生成气体的物质的量小于1mol;
故答案为:Cu+2H2SO4 (浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;小于1;
II.生成的二氧化硫有毒,是大气污染物,所以要进行处理,利二氧化硫为酸性还原性气体,酸性选③,还原性选①,
故答案为:①③.
点评 本题考查了Cu与浓硫酸的反应、二氧化硫的性质,题目难度不大,侧重于考查学生分析能力和实验能力,注意把握实验原理和尾气处理原理.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源:2017届吉林省高三上第二次模拟化学试卷(解析版) 题型:选择题
对于反应14CuSO4+5FeS2+12H2O===7Cu2S+5FeSO4+12H2SO4,下列说法正确的是
A.只有硫酸铜作氧化剂
B.SO42-既不是氧化产物又不是还原产物
C.被氧化的硫与被还原的硫的质量比为3∶7
D.1 mol硫酸铜可以氧化  mol的硫
mol的硫
查看答案和解析>>
科目:高中化学 来源:2017届广东省山一高三上第二次统测化学试卷(解析版) 题型:选择题
下列变化的实质相似的是( )
① 浓硫酸能在白纸上写字,氢氟酸能在玻璃上刻字
② 二氧化硫和氯气均能使品红溶液褪色
③ 二氧化硫能使高锰酸钾溶液、溴水褪色
④ 氨气和碘化氢气体均不能用浓硫酸干燥
⑤ 常温下浓硫酸可用铁容器存放、加热条件下浓硫酸能与木炭反应
⑥ 浓硫酸和浓盐酸在空气中敞口放置时浓度均减小
A.只有②③④ B.只有③⑤ C.只有③④⑥ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
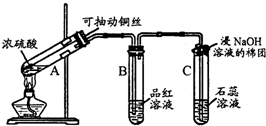
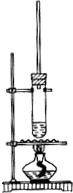 1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如右图.下列对该实验的描述错误的是( )
1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如右图.下列对该实验的描述错误的是( )| A. | 为了控制温度可以用水浴加热 | |
| B. | 长玻璃管起冷凝回流作用 | |
| C. | 加入过量乙酸可以提高1-丁醇的转化率 | |
| D. | 提纯乙酸丁酯可用饱和碳酸钠溶液洗涤 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
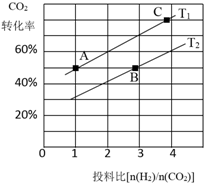 二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向.
二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向.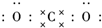 ,所含化学键的类型是共价键.
,所含化学键的类型是共价键.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 CH3COOC2H5+H2O;
CH3COOC2H5+H2O;查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高一9月月考化学卷(解析版) 题型:选择题
已知:①2FeCl3+2KI===2FeCl2+2KCl+I2;②2FeCl2+Cl2=2FeCl3。下列粒子的氧化性从强到弱的顺序正确的是
A.Cl2 >Fe3+>I2 B.I2>Cl2>Fe3+ C.Fe3+>Cl2>I2 D.Cl2>I2>Fe3+
>Fe3+>I2 B.I2>Cl2>Fe3+ C.Fe3+>Cl2>I2 D.Cl2>I2>Fe3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com