
(14分)现有碳酸钠和氯化钠的固体混合物,为了测定样品中碳酸钠的含量,化学兴趣小组同学分两组进行了以下实验。
第一组
实验装置
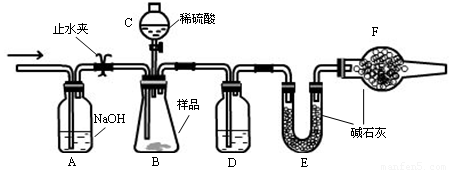
实验步骤
①连接好装置,检查气密性;
②盛装药品,其中样品a g,称量E的质量,连接好装置;
③关闭止水夹,向B中加入一定量稀硫酸;
④当B中充分反应后,打开止水夹,经过A装置,通入一定量的空气,将B、D中残余的气体全部赶入到E装置中;
⑤称量E,增重了b g 。
回答下列问题:
(1)仪器C的名称 ,D中盛放的试剂是 。
(2)B中发生反应的化学方程式为 。
(3)A中反应的离子方程式为 。
(4)改变下列一个条件,导致测定样品中的碳酸钠的质量百分含量偏低的是 (选填字母)
A.实验后期不通入空气 B.将仪器C中的硫酸换成盐酸
C.撤走仪器D D.撤走仪器F
第二组
实验装置
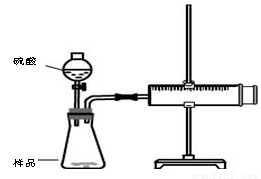
实验步骤
①检查装置气密性
②装好试剂,其中样品b g,连接好装置,将注射器的活塞推到底,即0mL处
③加入20mL硫酸,
④待反应充分进行后,活塞不在移动,记下活塞前端对应的刻度为V mL
回答下列问题
(1) 检查该装置气密性的方法是: 。
(2)对于产生气体的体积有两种观点,观点一:产生气体的体积为VmL;观点二:产生气体的体积为(V-20)mL,你认为 (填“观点一”“观点二”)正确。
(3)假如该实验在标准状况下进行,b=0.5g,V=76mL,则样品中碳酸钠的质量百分含量为 。
科目:高中化学 来源: 题型:
工业碳酸钠由于在生产过程中原料盐和工艺等的原因,常会含有Na2SO4、NaCl中的一种或两种杂质。现有工业碳酸钠样品,某化学兴趣小组就工业碳酸钠中是否含有这两种杂质进行探究。实验室有以下的仪器和药品可供使用:
烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹:1.0 mol·L-1H2SO4、1.0 mol·L-1HNO3、1.0mol·L-1HCl、NaOH稀溶液、0.1 mol·L-1AgNO3、0.1 mol·L-1BaCl2 、0.1 mol·LBa(NO3)2、蒸馏水。以下是部分实验探究过程:
1)提出假设:
假设1 白色粉末为 的混合物;
假设2 白色粉末为 的混合物;
假设3 白色粉末为碳酸钠、硫酸钠、氯化钠的混合物;
2)基于假设设计实验方案
3)根据实验方案进行实验
请回答:
(1)某同学取少许样品于试管中,加适量蒸馏水溶解,向试管中滴入0.1 mol·L-1的BaCl2溶液,有白色沉淀产生,他认为样品中含有Na2SO4。你认为他的结论是 (填“对的”或“错的”),原因是: 。
(2)设计实验方案
基于工业碳酸钠中两种杂质均存在这一假设,设计出实验方案(在答题卡上作答)。
| 编号 | 实验操作 | 预期现象和结论 |
| ① |
| 有无色气体产生,说明样品中含有Na2CO3。 若无气体产生,说明样品中没有Na2CO3。
|
| ② |
|
|
| ③ |
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:
(14分)现有碳酸钠和氯化钠的固体混合物,为了测定样品中碳酸钠的含量,化学兴趣小组同学分两组进行了以下实验。
第一组
实验装置
实验步骤
①连接好装置,检查气密性;
②盛装药品,其中样品a g,称量E的质量,连接好装置;
③关闭止水夹,向B中加入一定量稀硫酸;
④当B中充分反应后,打开止水夹,经过A装置,通入一定量的空气,将B、D中残余的气体全部赶入到E装置中;
⑤称量E,增重了b g 。
回答下列问题:
(1)仪器C的名称 ,D中盛放的试剂是 。
(2)B中发生反应的化学方程式为 。
(3)A中反应的离子方程式为 。
(4)改变下列一个条件,导致测定样品中的碳酸钠的质量百分含量偏低的是 (选填字母)
A.实验后期不通入空气 B.将仪器C中的硫酸换成盐酸
C.撤走仪器D D.撤走仪器F
第二组
实验装置
实验步骤
①检查装置气密性
②装好试剂,其中样品b g,连接好装置,将注射器的活塞推到底,即0mL处
③加入20mL硫酸,
④待反应充分进行后,活塞不在移动,记下活塞前端对应的刻度为V mL
回答下列问题
(1) 检查该装置气密性的方法是: 。
(2)对于产生气体的体积有两种观点,观点一:产生气体的体积为VmL;观点二:产生气体的体积为(V-20)mL,你认为 (填“观点一”“观点二”)正确。
(3)假如该实验在标准状况下进行,b=0.5g,V=76mL,则样品中碳酸钠的质量百分含量为 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年吉林省长春二中高一寒假质量检测化学试卷 题型:实验题
(14分)现有碳酸钠和氯化钠的固体混合物,为了测定样品中碳酸钠的含量,化学兴趣小组同学分两组进行了以下实验。
第一组
实验装置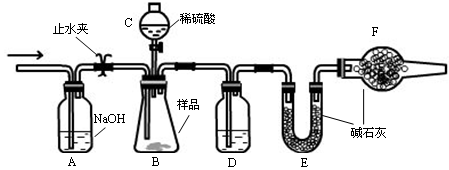
实验步骤
①连接好装置,检查气密性;
②盛装药品,其中样品a g,称量E的质量,连接好装置;
③关闭止水夹,向B中加入一定量稀硫酸;
④当B中充分反应后,打开止水夹,经过A装置,通入一定量的空气,将B、D中残余的气体全部赶入到E装置中;
⑤称量E,增重了b g 。
回答下列问题:
(1)仪器C的名称 ,D中盛放的试剂是 。
(2)B中发生反应的化学方程式为 。
(3)A中反应的离子方程式为 。
(4)改变下列一个条件,导致测定样品中的碳酸钠的质量百分含量偏低的是 (选填字母)
A.实验后期不通入空气 B.将仪器C中的硫酸换成盐酸
C.撤走仪器D D.撤走仪器F
第二组
实验装置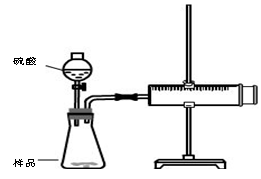
实验步骤
①检查装置气密性
②装好试剂,其中样品b g,连接好装置,将注射器的活塞推到底,即0mL处
③加入20mL硫酸,
④待反应充分进行后,活塞不在移动,记下活塞前端对应的刻度为V mL
回答下列问题
检查该装置气密性的方法是: 。
(2)对于产生气体的体积有两种观点,观点一:产生气体的体积为VmL;观点二:产生气体的体积为(V-20)mL,你认为 (填“观点一”“观点二”)正确。
(3)假如该实验在标准状况下进行,b=0.5g,V=76mL,则样品中碳酸钠的质量百分含量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O NH4Cl+NaHCO3(晶体)依据此原理,欲制得碳酸钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
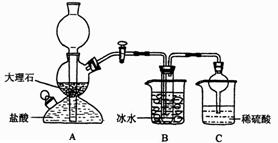
(1)A装置中所发生反应的离子方程式为 。
C装置中稀硫酸的作用为 。
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)

参照表中数据,请分析B装置中使用冰水是因为 。
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在 装置之间(填写字母)连接一个盛有 的洗气装置,其作用是 。
(4)利用改进后的装置进行实验,在B中的试管内析出了晶体,经必要的操作后得到了一种纯净的晶体。现有下列试剂:盐酸、浓氨水、生石灰、蒸馏水,利用本题所提供的试剂(只限一种)及试管、酒精灯等主要仪器,通过简单实验判断该晶体是碳酸氢钠晶体,而不是碳酸氢铵或食盐晶体,简述操作方法、实验现象及结论:
。
(5)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com