
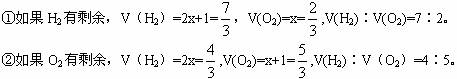
A.3∶4 B.4∶5 C.2∶1 D.2∶7
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解
| 序号 | 滴定前读数(mL) | 滴定后读数(mL) |
| 1 | 0.00 | 20.10 |
| 2 | 1.00 | 20.90 |
| 3 | 0.00 | 21.10 |
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:043
我国农业因遭受酸雨而造成每年损失高达15多亿元.为了有效控制酸雨,目前国务院已批准了《酸雨控制区和二氧化硫污染控制区划分方案》等法规.
(1)现有1份雨水样品,每隔一段时间测定该雨水样品的pH,所得数据如下:

分析数据,回答下列问题:
①雨水样品的pH变化的原因是(用化学方程式表示)_______________.
②如果将刚取样的上述雨水和自来水相混合,pH将变_______________,原因是(用化学方程式表示)_______________.
(2)你认为减少酸雨产生的途径可采用的措施是
①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
[ ]
(3)在英国进行的一个研究结果表明:高烟囱可以有效地降低地表面 浓度.在20世纪的60~70年代的10年间,由发电厂排放出的
浓度.在20世纪的60~70年代的10年间,由发电厂排放出的 浓度降低了35%,但由于建筑高烟囱的结果,地面
浓度降低了35%,但由于建筑高烟囱的结果,地面 浓度降低了30%之多.请你从全球环境保护的角度,分析这种方法是否可取.简述其理由.
浓度降低了30%之多.请你从全球环境保护的角度,分析这种方法是否可取.简述其理由.
(4)用传统的煤、石油作燃料,其主要缺点是什么?与传统的煤、石油燃料相比,哪种物质可作为新的能源?主要优点又是什么?
(5)为了防治酸雨,降低煤燃烧时向大气排放 ,工业上常将生石灰和含硫煤混合后使用.请写出燃烧时,有关“固硫”(不使硫化合物进入大气)反应的化学方程式:_______________.并比较此法与将“石灰石粉末与含硫煤混合”便可防治酸雨的方法,哪个更好些?_____________(填“生石灰”或“石灰石法”).
,工业上常将生石灰和含硫煤混合后使用.请写出燃烧时,有关“固硫”(不使硫化合物进入大气)反应的化学方程式:_______________.并比较此法与将“石灰石粉末与含硫煤混合”便可防治酸雨的方法,哪个更好些?_____________(填“生石灰”或“石灰石法”).
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(12分)四氧化三铁纳米微粒可用于涂料、油墨、隐身材料、磁记录、电极材料、催化剂等多领域,实验室可用如下的方法来制备这种材料并进行检测。
Ⅰ.制备
(1)溶解、沉淀操作中不断通入氮气有两个作用:①是通过在反应过程中通入气体形成微型气泡,将刚生成的四氧化三铁微粒包围,来阻止微粒的长大或聚集成团;② ▲ 。
(2)操作Ⅲ的名称是________▲___ 。
Ⅱ.产品检测
一、定性检测:产品中铁元素价态检测
试剂主要有:3mol/L硫酸、0.1mol/L氢氧化钠溶液、20%硫氰化钾溶液、0.01mol/L酸性高锰酸钾溶液、氯水 (其它用品任选)
(3)请选用上述试剂完成下表
| 步骤 | 操作 | 现象、结论 |
| 1 | ▲ |
|
| 2 | 取少量产品于试管中加适量步骤1处理好溶液溶解,配成溶液 | 固体溶解,溶液呈浅黄色 |
| 3 | 取少量步骤2配好溶液于试管中,滴加几滴20%硫氰化钾溶液,振荡 | ▲ ,产品含有Fe3+ |
| 4 | ▲ | ▲ ,产品含有Fe2+ |
二、定量测定:
称取23.2g样品于烧杯中,加入加热煮沸后的稀硫酸充分溶解,并不断加热、搅拌,待固体完全溶解后,向所得溶液中加入10.0 g铜粉充分反应后过滤、洗涤、干燥得剩余固体3.6g。取滤液体积的1/10用浓度为0.200 mol·L-1的酸性KMnO4滴定,至终点时消耗KMnO4溶液体积29.80mL。
(4)产品中Fe3+和Fe2+的物质的量之比为 ▲ 。
III.结果讨论
(5)产品中Fe3+和Fe2+的物质的量之比略大于2:1的可能原因是 ▲ 。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年重庆市高三上学期12月月考理综化学试卷(解析版) 题型:填空题
硫元素有多种化合价,可形成多种化合物。
(1)常温下用1 mol·L﹣1 100 mL NaOH溶液恰好完全吸收0.1 mol SO2气体,此反应的离子方程式为 ;该溶液pH_______7(填“=”“>”或“<”)。
(2)某同学在常温下设计如下实验流程探究Na2S2O3的化学性质。

实验①可说明________(填字母)
A.该Na2S2O3溶液中水电离的c(OH﹣)=10﹣8mol/L
B.H2S2O3是一种弱酸
C.Na2S2O3是一种弱电解质
D.Na2S2O3水解方程式为S2O32﹣+2H2O=H2S2O3+2OH﹣
写出实验②发生反应的离子方程式 。
(3)实验室制得的Na2S2O3粗晶体中往往含有少量杂质。为了测定粗产品中Na2S2O3·5H2O(摩尔质量为248g/mol)的含量,一般采用在酸性条件下用KMnO4标准液滴定的方法(假定粗产品中杂质与酸性KMnO4溶液不反应)。称取1.28 g的粗样品溶于水,用0.40mol/L KMnO4溶液(加入适量硫酸酸化)滴定,当溶液中S2O32﹣全部被氧化时,消耗KMnO4溶液体积20.00 mL。(已知:5S2O32﹣+8MnO4﹣+14H+=8Mn2++10SO42﹣+7H2O)。
试回答:
①KMnO4溶液置于——(填“酸式”或“碱式”)滴定管中,滴定终点的现象为 。
②若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O3·5H2O的质量分数的测量结果_____________(填“偏高”“偏低”或“不变”)。
③产品中Na2S2O3·5H2O的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年江苏省淮安市高三第四次调研测试化学试卷 题型:实验题
(12分)四氧化三铁纳米微粒可用于涂料、油墨、隐身材料、磁记录、电极材料、催化剂等多领域,实验室可用如下的方法来制备这种材料并进行检测。
Ⅰ.制备

(1)溶解、沉淀操作中不断通入氮气有两个作用:①是通过在反应过程中通入气体形成微型气泡,将刚生成的四氧化三铁微粒包围,来阻止微粒的长大或聚集成团;② ▲ 。
(2)操作Ⅲ的名称是________▲___ 。
Ⅱ.产品检测
一、定性检测:产品中铁元素价态检测
试剂主要有:3mol/L硫酸、0.1mol/L氢氧化钠溶液、20%硫氰化钾溶液、0.01mol/L酸性高锰酸钾溶液、氯水 (其它用品任选)
(3)请选用上述试剂完成下表
|
步骤 |
操作 |
现象、结论 |
|
1 |
▲ |
|
|
2 |
取少量产品于试管中加适量步骤1处理好溶液溶解,配成溶液 |
固体溶解,溶液呈浅黄色 |
|
3 |
取少量步骤2配好溶液于试管中,滴加几滴20%硫氰化钾溶液,振荡 |
▲ ,产品含有Fe3+ |
|
4 |
▲ |
▲ ,产品含有Fe2+ |
二、定量测定:
称取23.2g样品于烧杯中,加入加热煮沸后的稀硫酸充分溶解,并不断加热、搅拌,待固体完全溶解后,向所得溶液中加入10.0 g铜粉充分反应后过滤、洗涤、干燥得剩余固体3.6 g。取滤液体积的1/10用浓度为0.200 mol·L-1的酸性KMnO4滴定,至终点时消耗KMnO4溶液体积29.80mL。
(4)产品中Fe3+和Fe2+的物质的量之比为 ▲ 。
III.结果讨论
(5)产品中Fe3+和Fe2+的物质的量之比略大于2:1的可能原因是 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com