
���� ��1�������ڿ����е�Ư���ѱ��ʣ���ˮ��������̼��Ӧ����̼��ơ�HClO��
��2��FeSO4��Һ��ϡH2SO4�ữ������һ��ʱ������Ի�ɫ����Ӧ�����������������еμ�KI-������Һ����ɫ����������������ӷ���������ԭ��Ӧ���ɵ⣮
��� �⣺��1�������ڿ����е�Ư���ѱ��ʣ���ˮ��������̼��Ӧ����̼��ơ�HClO�������ķ�ӦΪCa��ClO��2+CO2+H2O=CaCO3+2HClO��2HClO$\frac{\underline{\;����\;}}{\;}$2HCl+O2����
�ʴ�Ϊ��Ca��ClO��2+CO2+H2O=CaCO3+2HClO��2HClO$\frac{\underline{\;����\;}}{\;}$2HCl+O2����
��2��FeSO4��Һ��ϡH2SO4�ữ������һ��ʱ������Ի�ɫ����Ӧ���������������ӷ�ӦΪ4Fe2++4H++O2=4Fe3++2H2O�������еμ�KI-������Һ����ɫ����������������ӷ���������ԭ��Ӧ���ɵ⣬���ӷ�ӦΪ2Fe3++2I-=2Fe2++I2���ʴ�Ϊ��4Fe2++4H++O2=4Fe3++2H2O��2Fe3++2I-=2Fe2++I2��
���� ���⿼�����ӷ�Ӧ����ѧ��Ӧ����д��Ϊ��Ƶ���㣬���շ����ķ�Ӧ�����ӷ�Ӧ����д����Ϊ���Ĺؼ�������������ԭ��Ӧ�Ŀ��飬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ͬ�Ļ�ѧ��Ӧ���ȿ��ܲ�ͬ | |
| B�� | ����ͨ���ı��¶������ƻ�ѧ��Ӧ���� | |
| C�� | ����ͨ���ӳ���ѧ��Ӧ��ʱ�����ı仯ѧ��Ӧ���� | |
| D�� | һ����ѧ��Ӧ��һ�������´ﵽ��ʱ�������淴Ӧ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | X��ԭ�Ӱ뾶��Y�Ĵ� | B�� | Xԭ�ӵ�������������Y�Ĵ� | ||
| C�� | X��ԭ��������Y��С | D�� | XԪ�ص�������۱�Y�Ĵ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
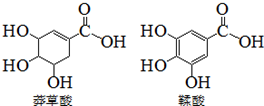 ç������һ�ֺϳ�ҩ���Ƶ�ԭ�ϣ����������ƻ������ʯ���ֲ���У����й����������л��������˵����ȷ���ǣ�������
ç������һ�ֺϳ�ҩ���Ƶ�ԭ�ϣ����������ƻ������ʯ���ֲ���У����й����������л��������˵����ȷ���ǣ�������| A�� | �����������Ȼ�����Һ����ɫ | |
| B�� | ������ӱ�ç������Ӷ�����˫�� | |
| C�� | �����ʵ�������������NaOH��Ӧ������NaOH������ͬ | |
| D�� | �����ᶼ������ˮ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����β���з����Ĵ�ת����Ӧ��2NO+2CO$\frac{\underline{\;����\;}}{\;}$N2+2CO2 | |
| B�� | ��ҵ��������MnO2+4HCl��Ũ�� $\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O | |
| C�� | ȼúʱ����ʯ��ʯ����SO2�ŷţ�2CaCO3+2SO2+O2$\frac{\underline{\;����\;}}{\;}$2CaSO4+2CO2 | |
| D�� | ��Na2CO3��Һ����ˮ���еIJ�����CaSO4��CaSO4+CO32-�TCaCO3+SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֬�Dz���������ߵ�Ӫ������ | |
| B�� | ���ܷ���������Ӧ | |
| C�� | ��ά�ؿ�������������ˮ��������� | |
| D�� | �Ȱ�������к���2�ֹ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaOH | B�� | Ba��OH��2 | C�� | KSCN | D�� | BaCl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | x=10ʱ����Һ����NH4+��Al3+��SO42-����c��NH4+��=c��Al3+�� | |
| B�� | x=20ʱ����Һ���������ķ�Ӧ���ӷ���ʽΪ��Al3++2SO42-+2Ba2++4OH-�T2BaSO4��+AlO2-+2H2O | |
| C�� | x=30ʱ����Һ����Ba2+��AlO2-��OH-����c��OH-����c��AlO2-�� | |
| D�� | �μӹ����У����ɳ�����������ʵ���Ϊ0.003mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com